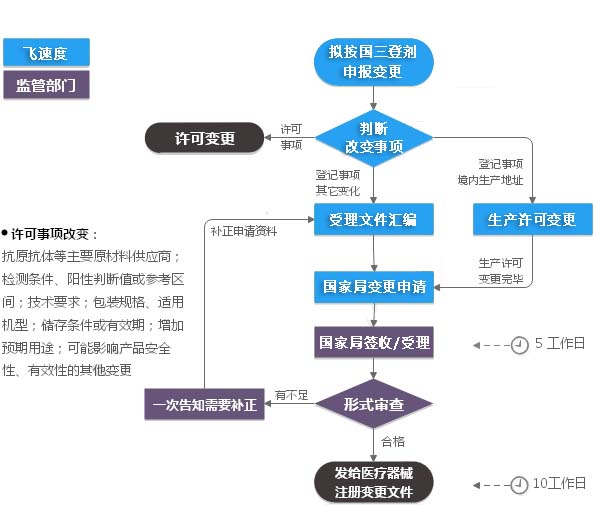
依据《
体外诊断试剂注册管理办法》关于三类医疗器械(体外诊断试剂)注册证变更相关规定,注册证及其附件载明的内容发生变化时,注册人应当向原注册部门(药监总局)申请注册变更。
许可事项变更包括哪些事项
1、抗原、抗体等主要原材料的供应商;
2、检验方法,阳性判断值或参考区间;
3、产品技术要求中的性能指标和检验方法;
4、包装规格、适用机型;
5、产品储存条件或有效期;
6、预期用途,如增加适用样本类型或适用人群;
7、可能影响产品安全性、有效性的其他变更。
注意:
1、抗原、抗体等主要原材料本身的变化,如变更生产商且抗原、抗体性质发生变化的情况不属于许可变更事项。
2、增加适用样本类型,增加适用人群或者其他由于主要原材料供应商、检验方法、分析性能等变化影响产品临床性能的变更情况原则上应提交
临床试验资料。
3、对于同时发生多项或者先后发生多次变更的情况,需要注意考虑以及评价这些变更对产品安全有效性的整体综合或者累积影响。
三类IVD注册证许可事项变更申报资料
1、《体外诊断试剂注册变更(许可事项)申请表》
(1)应有法定代表人或负责人签字并加盖公章。
(2)所填写项目应齐全、准确,变更前后情况清晰、明确。
2、证明性文件
(1)企业营业执照副本复印件,且应在有效期内。
(2)组织机构代码证复印件,且应在有效期内。
3、注册人关于变更情况的声明
(1)变更的原因及目的说明。
(2)变更可能对产品性能产生影响的技术分析。
(3)与产品变化相关的产品风险分析资料。
4、原医疗器械注册证及其附件复印件、历次医疗器械注册变更文件复印件。
5、变更申请项目申报资料(资料中涉及需要提交产品技术要求、说明书的,另需提交Word文档形式的电子文本,并提交电子文本与产品技术要求变化对比表、说明书完全一致的声明)
(1)变更抗原、抗体等主要材料的供应商,应当提交下列资料:
Ⅰ、变更后抗原、抗体等主要材料的研究资料。
Ⅱ、分析性能评估资料。
Ⅲ、临床试验资料。
Ⅳ、变更前、后的产品技术要求、产品说明书。
(2)变更检测条件、阳性判断值或参考区间,应当提交下列资料:
Ⅰ、变更后的检测条件、阳性判断值或参考区间确定的详细试验资料。
Ⅱ、临床试验资料。
Ⅲ、变更前、后的产品技术要求、产品说明书。
(3)变更产品储存条件和/或有效期,应当提交下列资料:
Ⅰ、有关产品稳定性研究的试验资料。
Ⅱ、变更前、后的产品技术要求、产品说明书及标签样稿。
(4)修改产品技术要求,但不降低产品有效性的变更,应当提交下列资料:
Ⅰ、有关分析性能评估的试验资料。
Ⅱ、变更前、后的产品技术要求、产品说明书。
(5)对产品说明书和/或产品技术要求中文字的修改,但不涉及技术内容的变更,应当提交下列资料:
Ⅰ、产品说明书和/或产品技术要求的更改情况说明,说明中应当包含变更情况对比表及电子文本(Word文档)。
Ⅱ、变更前、后的产品说明书和/或产品技术要求。
(6)变更包装规格,应当提交下列资料:
Ⅰ、变更前、后的产品技术要求、产品说明书和标签样稿(如涉及)。
Ⅱ、判断变更的包装规格与已上市包装规格间是否存在性能差异,如存在产品性能差异,需要提交采用变更的包装规格产品进行分析性能评估的试验资料;如产品性能无差异,需要提交变更的包装规格与已上市包装规格之间不存在性能差异的详细说明,具体说明不同包装规格之间的差别及可能产生的影响。
(7)变更适用机型,应当提交下列资料:
Ⅰ、采用新的适用机型进行分析性能评估的试验资料。
Ⅱ、提供变更前、后的产品技术要求、产品说明书和标签样稿(如涉及)。
(8)增加临床适应症的变更,应当提交下列资料:
Ⅰ、针对增加的临床适应症所进行的分析性能评估资料(如涉及)。
Ⅱ、针对增加的临床适应症所进行的临床试验资料。
Ⅲ、变更前、后的产品技术要求、产品说明书。
(9)增加临床测定用样本类型的变更,应当提交下列资料:
Ⅰ、采用增加的临床测定样本类型与已批准的样本类型进行比对的临床试验资料,如增加的样本类型与原批准的样本类型无直接可比性,可以选择与样本类型具可比性的已上市同类产品进行比对的临床试验。
Ⅱ、变更前、后的产品技术要求、产品说明书。
(10)其他可能影响产品有效性的变更,根据变更情况提供有关变更的试验资料。
(11)应当根据产品具体变更情况,提交该变更对产品性能可能产生的影响进行验证的试验资料(如涉及)。
6、符合性声明
(1)注册人声明本产品符合《体外诊断试剂注册管理办法》和相关法规的要求;声明本产品符合现行国家标准、行业标准,并提供符合标准的清单。
(2)所提交资料真实性的自我保证声明(境内产品由注册人出具)。
7、申办人身份证复印件。申办人不是营业执照载明的法定代表人或负责人的,应提交法定代表人或负责人的授权委托书。
注册变更不适用的情况
1、产品基本反映原理变更;
2、产品阳性判断值或者参考区间改变,并且具有新的临床诊断意义:如预期用途或者使用目的;
3、其他对产品安全有效性产生重大影响的改变。
注意:
1、产品的设计、组成、主要原材料(如抗原抗体、引物探针)、关键反应成分、量值溯源、结果判读等发生实质性改变原则上不属于许可事项变更。
2、降低产品的安全有效性,为应对已知的风险、不良事件等显著改变产品的分析性能或临床性能的情况原则上不属于许可事项变更。
三类IVD注册变更客户咨询问题解答
1、三类注册的体外诊断试剂,变更适用机型后,注册证的日期信息会有变化吗?比如之前是2019年注册的,如果2020年新增了适用机型,那么注册证日期是2019开始还是2020开始呢?
答:注册证变更不影响注册证号及日期。