24小时服务热线:19103801095
ONE-STOP SERVICE
SERVICE PROCESS

精准客户咨询/再咨询

分析产品是否可做

客户产品市场调研

制定可行性方案

签订服务合同

启动项目整体方案

客户回访满意度评价

领取注册证/生产许可证

编制注册资料及发补

现场指导体系布局

临床试验项目启动

协助客户产品送检
免费赠送3万家医疗器械企业名录
SELECTED CASES

白介素6(IL-6)检测试剂盒(荧光免疫层析法)临床验证案例

一次性高频消融电极(手术高频电刀)注册体系辅导案例

中频治疗仪(中频电疗仪)注册GMP体系案例

细菌性阴道病检测试剂盒(唾液酸酶法)临床验证案例

医用隔离眼罩(医用防护眼镜)备案案例

医用一次性使用防护服注册临床评价案例

额温枪(额温计)产品注册临床验证案例

一次性使用医用外科口罩产品注册案例

一次性使用静脉留置针临床试验案例

血小板聚集功能(ADP途径)检测试剂盒临床验证案例

血小板聚集功能(AA途径)检测试剂盒临床验证案例

血栓弹力图(普通杯)检测试剂盒临床验证案例

全自动化学比浊测定仪注册案例

血栓弹力图仪注册GMP体系案例

医用液体伤口敷料备案案例

光学相干层析成像激光宫颈检测仪临床试验案例

北京飞速度医疗科技有限公司总部设立于北京,全国下设10余家分子公司,为全球生物制药行业、医疗器械生产企业,提供全方位、一站式医疗技术外包服务。公司拥有200余人的硕博专业技术团队,为600余家药品和医疗器械生产企业提供药物临床前研究、安全性验证、动物试验、真实世界研究、药物Ⅰ期和Ⅱ、Ⅲ期临床试验、医疗器械临床试验、产品注册申报、GMP认证等外包研究服务。
为800余家医疗机构提供国家临床试验机构审批、医疗机构制剂审批、医疗机构等级评审、国家及省级重点科室建设、胸痛中心、卒中中心、创伤中心等技术咨询服务。
飞速度秉承“助力科技,让生命更美好”的发展理念,致力于为客户提供优质的服务与个性化的解决方案,为客户降低研发风险、节约研发成本、降低研发难度、缩短产品市场化进程,让客户少走弯路。

2020年度优秀经营企业证书

中国医疗器械行业协会会员

AAA级质量服务诚信单位

郑州医疗器械协会副会长单位

ISO9001质量管理体系认证证书
 专业团队
专业团队顶尖的法规专家带队,具备丰富经验
 一站服务
一站服务产品研发到上市,全流程服务
 质量保证
质量保证全程质控团队监管,确保万无一失
 售后无忧
售后无忧服务满意度回访,造就行业标杆
NEWS INFORMATION
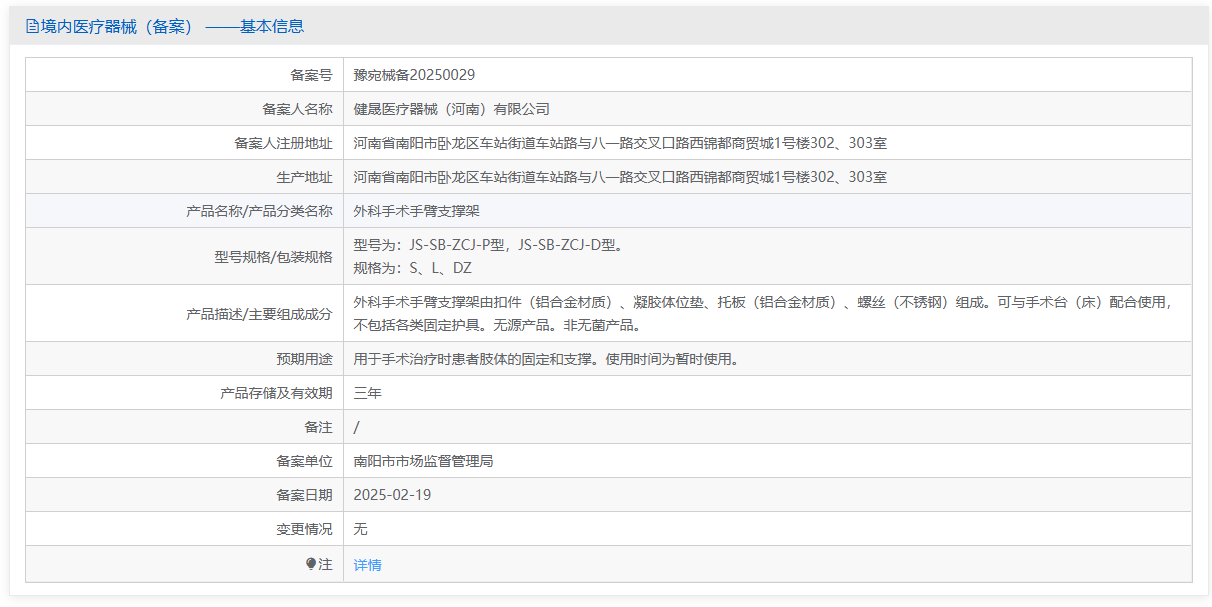 第一类医疗器械外科手术手臂支撑架备案办理流程及步骤周期指南
第一类医疗器械外科手术手臂支撑架备案办理流程及步骤周期指南
外科手术手臂支撑架由导轨固定夹、不锈钢固定直杆、万向支臂、臂托、臂托垫组成。其中臂托垫采用高分子材料制成,其他组件采用金属材料制成。在使用过程中不接触中枢神
 第二类医疗器械赘疣套扎套装注册办理流程及步骤周期指南
第二类医疗器械赘疣套扎套装注册办理流程及步骤周期指南
赘疣套扎套装由3个赘疣套扎贴和1个套扎夹组成,其中赘疣套扎贴由水刺聚酯无纺布医用胶带、双面医用胶带、聚甲醛圆盘、硅化纸衬片、透明PET聚酯衬片组成,非无菌提供。通
 第二类医疗器械血管吻合用隔离垫片注册办理流程及步骤周期指南
第二类医疗器械血管吻合用隔离垫片注册办理流程及步骤周期指南
血管吻合用隔离垫片为长方形片状物,采用硅橡胶材料制成,呈绿色,为一次性使用无菌产品。用于血管吻合时,隔离待缝合血管与周围组织,为医生观察待缝合血管提供更为清晰的
 第二类医疗器械移植用脂肪过滤装置套装注册办理流程及步骤周期指南
第二类医疗器械移植用脂肪过滤装置套装注册办理流程及步骤周期指南
移植用脂肪过滤装置套装由过滤装置、导管夹、出口管、废液袋、鲁尔接头、进口管、穿刺针头、保护套组成。无菌提供,一次性使用。用于脂肪移植手术时,过滤掉取自人体的脂
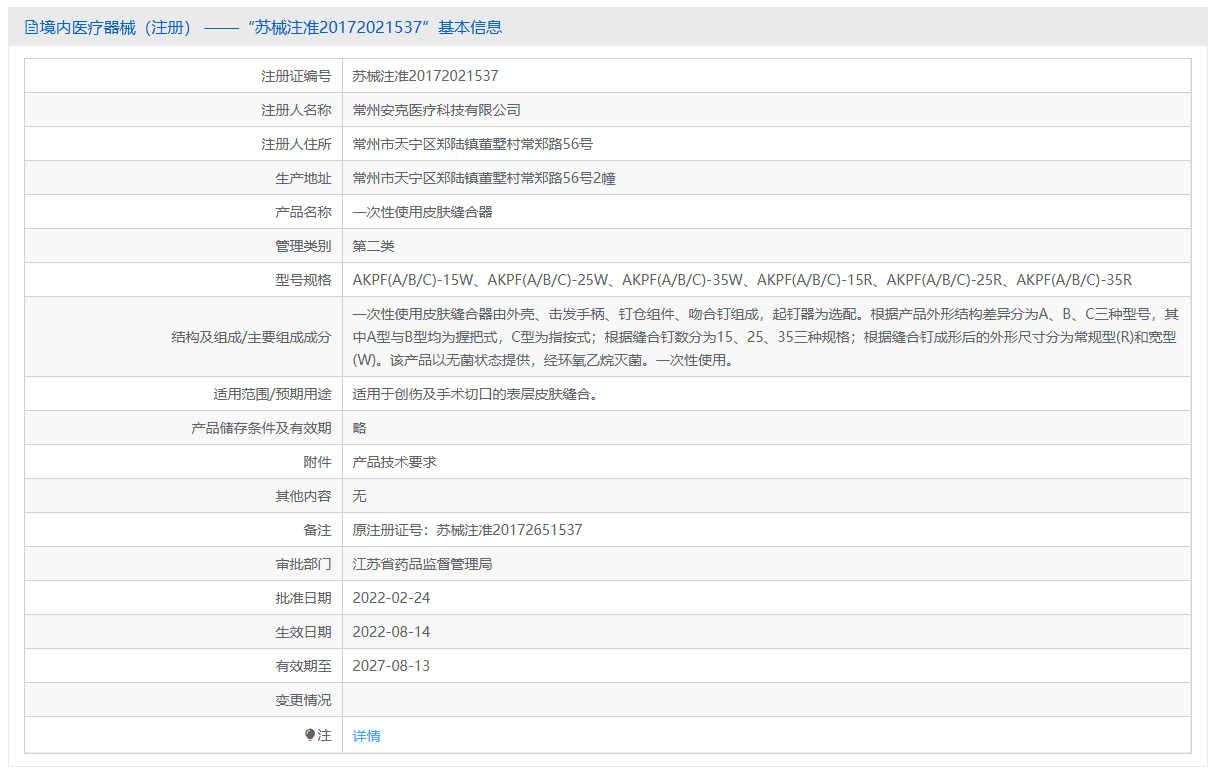 第二类医疗器械一次性使用创口辅助缝合器注册办理流程及步骤周期指南
第二类医疗器械一次性使用创口辅助缝合器注册办理流程及步骤周期指南
一次性使用创口辅助缝合器由外壳、主轨、针托、1.25mm穿刺针(带引线槽)、拖线钮、定位胶垫组成,不包含缝合线。穿刺针采用不锈钢材料制成,其它部分采用高分子材料制成。
 第三类医疗器械微型皮片扩展载片敷料及软木盘注册办理流程及步骤周期指南
第三类医疗器械微型皮片扩展载片敷料及软木盘注册办理流程及步骤周期指南
微型皮片扩展载片敷料及软木盘由扩展载片敷料(铝箔基片+聚酰胺纱布,已预折叠)和软木盘(木材制成)组成,无菌提供,一次性使用。与烧伤植皮机、粘合剂配合,用于分离和扩展皮岛
 云南省26年4月份共批准注册境内第二类医疗器械产品6个(附名单)
云南省26年4月份共批准注册境内第二类医疗器械产品6个(附名单)
2026年4月,云南省药品监督管理局共批准注册境内第二类医疗器械产品6个(具体产品见附件)。 特此公告。 附件:2026年4月批准注册境内第二类医疗器械产品目录 云南
 2026年最新湖北省第二类医疗器械注册申报操作手册
2026年最新湖北省第二类医疗器械注册申报操作手册
1.相关配置 1.1.环境要求 1.1.1.浏览器 IE11及以上版本浏览器,以IE11文本模式进行浏览;谷歌浏览器、360浏览器(极速模式)。 2.业务申报 2.1.注册登录
 湖北省26年4月份共批准注册第二类医疗器械产品35个(附名单)
湖北省26年4月份共批准注册第二类医疗器械产品35个(附名单)
根据《医疗器械注册与备案管理办法》、《体外诊断试剂注册与备案管理办法》相关规定,2026年4月湖北省药品监督管理局共批准注册医疗器械产品35个。 特此公告。 附
 湖南省26年4月份共批准首次注册第二类医疗器械产品53个(附名单)
湖南省26年4月份共批准首次注册第二类医疗器械产品53个(附名单)
2026年4月,湖南省药品监督管理局共批准首次注册第二类医疗器械产品53个,新开办生产企业4家(具体产品和企业见附件)。 特此公告。 附件:1.湖南省药品监督管理局2026年
 广西药监局26年4月份批准注册第二类医疗器械产品信息(附名单)
广西药监局26年4月份批准注册第二类医疗器械产品信息(附名单)
根据《医疗器械监督管理条例》相关规定,现将2026年4月广西药监局审批的第二类医疗器械产品注册信息予以公布。 文件下载:2026年4月第二类医疗器械产品注册信息表.xls
 江苏省26年4月份共批准注册第二类医疗器械产品168个(附名单)
江苏省26年4月份共批准注册第二类医疗器械产品168个(附名单)
2026年4月,江苏省药品监督管理局共批准注册第二类医疗器械产品168个(具体产品见附件)。 特此公告。 附件:2026年4月批准注册第二类医疗器械产品目录、技术审评报告
 飞速度CRO助力华之源完成国内首款单管五联检高血压用药基因检测试剂盒获批 !
飞速度CRO助力华之源完成国内首款单管五联检高血压用药基因检测试剂盒获批 !
在2026年1月20日这个我国精准医疗领域被赋予特殊意义的重要时刻,河南省华之源生物技术有限公司所研发的那一款以快速多色探针熔解曲线这一具备创新性的专利技术作为核心
 飞速度助力安诺优达的阿尔兹海默病血检试剂盒p-tau181正式获批!
飞速度助力安诺优达的阿尔兹海默病血检试剂盒p-tau181正式获批!
继阿尔兹海默病血检试剂盒Aβ1-42成功获批后,安诺优达又一血检试剂盒“磷酸化tau-181 蛋白测定试剂盒(磁微粒荧光发光法)”(京械注准20252400969)正式获得
 飞速度临床事业部总监在郑州市医疗器械生产企业自查报告培训授课,反响热烈!
飞速度临床事业部总监在郑州市医疗器械生产企业自查报告培训授课,反响热烈!
2024年3月7日,郑州市市场监督管理局联合郑州医疗器械行业协会,在郑州颐和医院颐和会堂举办“郑州市医疗器械生产企业自查报告培训”。郑州市市场监督管理局医疗器械
 2023年云时代&飞速度联合客户答谢会圆满完成!
2023年云时代&飞速度联合客户答谢会圆满完成!
2023年12月23日,由云时代医疗器械供应链(河南) 有限公司&北京飞速度医疗科技有限公司联合举办的2023年终客户答谢会”隆重举行。来自省内外各地的客户、合作伙伴齐聚一
 飞速度助力洛阳市孟津人民医院召开国家临床试验机构备案启动会圆满举行!
飞速度助力洛阳市孟津人民医院召开国家临床试验机构备案启动会圆满举行!
为提高医院科研能力,掌握临床试验方法和技术,积极推进临床试验项目备案工作,进一步增强医院综合实力。9月7日下午,洛阳市孟津人民医院在老院区综合病房楼11楼大会议室召开国家临
 临近月底,飞速度再次中标临床试验机构备案项目,中标130万元!
临近月底,飞速度再次中标临床试验机构备案项目,中标130万元!
昨日,飞速度刚发布《本月,飞速度成功拿下三家临床试验机构备案项目,总额高达500万!》的新闻,今日再次传来好消息,临近月底飞速度再次中标一家临床试验机构备案项目,中标淄博市
 吻合口加固片注册审查指导原则 (征求意见稿)
吻合口加固片注册审查指导原则 (征求意见稿)
本指导原则旨在指导注册申请人对吻合口加固片注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则系对吻合口加固片注册申报资料的
 血浆分离器及血浆成分分离器注册审查指导原则(征求意见稿)(2026年版)
血浆分离器及血浆成分分离器注册审查指导原则(征求意见稿)(2026年版)
本指导原则旨在帮助和指导注册申请人对血浆分离器及血浆成分分离器注册申报资料进行准备,同时也为技术审评部门提供参考。 本指导原则是对血浆分离器及血浆成分分离器
 一次性使用心脏停跳液灌注器注册审查指导原则(征求意见稿)(2026年版)
一次性使用心脏停跳液灌注器注册审查指导原则(征求意见稿)(2026年版)
本指导原则旨在指导注册申请人对一次性使用心脏停跳液灌注器(以下简称“灌注器”)产品的注册申报资料进行准备及撰写,同时也为技术审评部门对注册申报资料的审
 乳房旋切穿刺针及配件注册审查指导原则(征求意见稿)(2026年版)
乳房旋切穿刺针及配件注册审查指导原则(征求意见稿)(2026年版)
本指导原则旨在帮助和指导注册申请人对乳房旋切穿刺针及配件注册申报资料进行准备,同时也为技术审评部门提供参考。 本指导原则是对乳房旋切穿刺针及配件注册申报资料
 可吸收结扎夹注册审查指导原则(征求意见稿)(2026年版)
可吸收结扎夹注册审查指导原则(征求意见稿)(2026年版)
本指导原则旨在指导注册申请人对可吸收结扎夹产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对可吸收结扎夹产品注册申
 人工颈椎间盘假体注册审查指导原则 (2025年修订)(征求意见稿)
人工颈椎间盘假体注册审查指导原则 (2025年修订)(征求意见稿)
本指导原则旨在指导注册申请人对人工颈椎间盘假体注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供技术参考。 本指导原则是对人工颈椎间盘假
COOPERATION CUSTOMER

乐普(北京)医疗器械股份有限公司

英国BTL医疗实业集团

河南优德医疗设备股份有限公司

博硕科技(江西)有限公司

河南秦江医疗器械有限公司

视微影像(河南)科技有限公司

郑州光超医疗科技有限公司

北京创元成业科技有限公司

新疆西能韦尔电气有限公司

郑州华航科技股份有限公司

深圳市锦瑞生物科技有限公司

北京伏尔特技术有限公司

河南驼人医疗器械集团有限公司

贵州省药材有限责任公司

河南德源祥生物科技有限公司

河南民生智能医疗技术股份有限公司

广东埃纳生医学科技有限公司

河南亚都实业有限公司

济南奥倍康医疗科技发展有限公司

郑州金象义齿模型制作有限公司

河南省超亚医药器械有限公司

河南省生茂医疗设备有限公司

杭州得道医疗设备科技有限公司

豪孚迪医疗器械(上海)有限公司

浙江世纪康大医疗科技股份有限公司

河南智佐生物科技有限公司

北京天恩泽基因科技有限公司

苏州晨曦生物科技有限公司

郑州申友生物技术有限公司

郑州普湾医疗技术有限公司

河南沃迈生物科技有限公司

河南曙光健士医疗器械集团有限公司

重庆高圣生物医药有限责任公司

山西康宝生物科技有限公司

郑州人福博赛生物技术有限责任公司

郑州邦奇生物技术有限公司