根据《
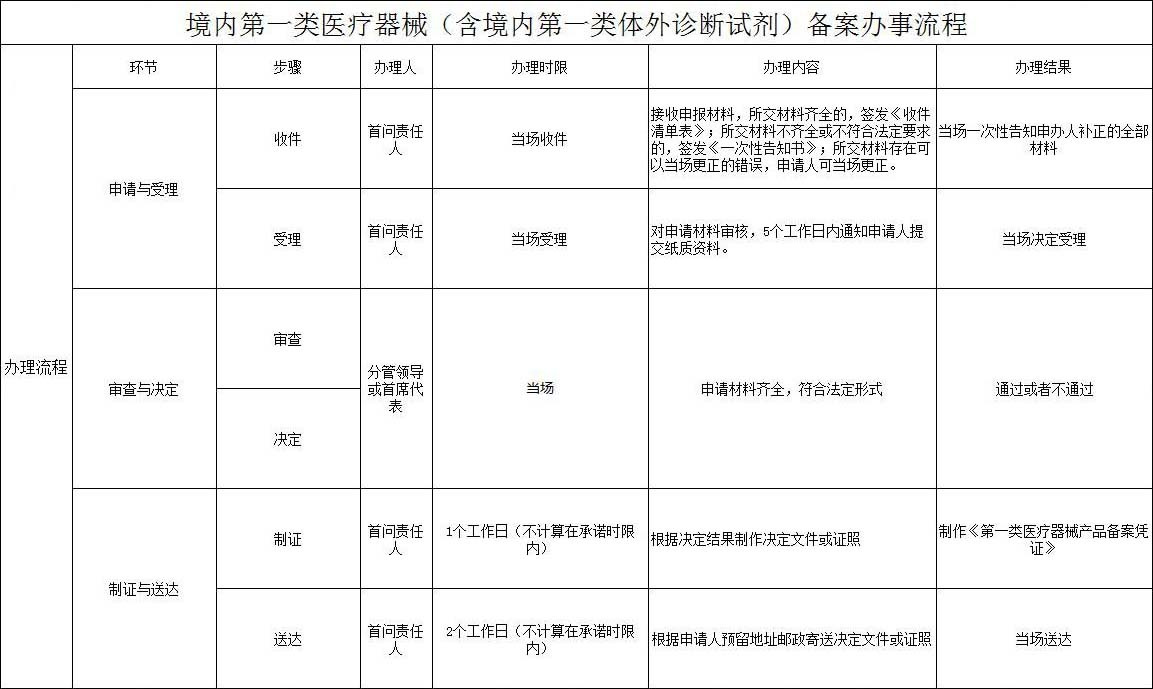
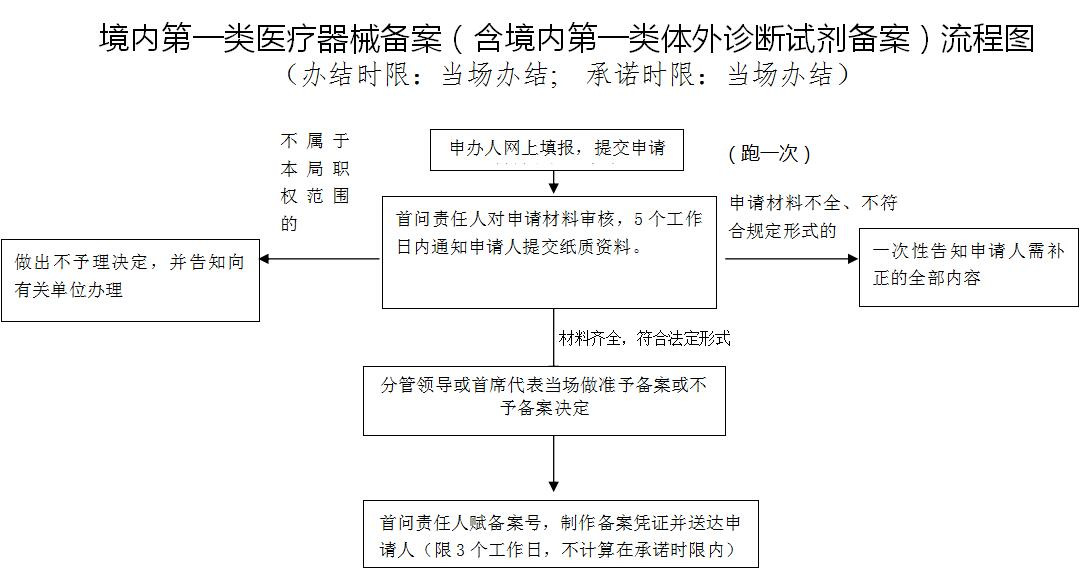
体外诊断试剂注册管理办法》(局令5号)的规定,第一类体外诊断试剂实行备案管理,体外诊断试剂备案是备案人向药监管理部门提交备案资料,药监管理部门对提交的备案资料存档备查。
备案资料符合要求的,药监管理部门应当当场备案;备案资料不齐全或者不符合规定形式的,应当一次告知需要补正的全部内容,由备案人补正后备案。对备案的体外诊断试剂,药监管理部门应当按照相关要求的格式制作备案凭证,并将备案信息表中登载的信息在其网站上予以公布。
注意:已备案的体外诊断试剂管理类别调整的,备案人应当主动向食品药品监督管理部门提出取消原备案;
第一类IVD(产品备案)申报资料
(一)《第一类医疗器械备案表》;
(二)安全风险分析报告;
(三)产品技术要求;
(四)产品检验报告;
(五)临床评价资料;
(六)产品说明书及最小销售单元标签设计样稿;
(七)生产制造信息;
(八)证明性文件(原件):1、企业营业执照;2、组织机构代码;
(九)符合性声明:
1、声明符合医疗器械备案相关要求;
2、声明本产品符合第一类医疗器械产品目录或相应体外诊断试剂分类子目录的有关内容;
3、声明本产品符合现行国家标准、行业标准并提供符合标准的清单;
4、声明所提交备案资料的真实性。