24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

在体外诊断领域,为了提高试剂的适用性和准确性,不断有新的适用仪器与体外诊断试剂配套使用。本文将着重描述体外诊断试剂增加配套使用的仪器,重点关注新增仪器与已批准仪器
查看详情
前言: 临床试验机构备案,是指医疗器械和药物临床试验机构按照相关规定的条件和要求,将机构概况、专业技术水平、组织管理能力、伦理审查能力等信息提交食品药品监督管理部门
查看详情
氧气是维持人体生命正常进行的重要物质,而人体获得氧气的最基本途径是呼吸。呼吸是不断地把空气中的氧气吸入体内,再把体内的二氧化碳排出体外的过程。呼吸又分为外呼吸和
查看详情
在眼科中高端设备领域,眼科OCT设备、全飞秒激光设备、眼科手术显微镜、超乳玻切一体机、眼底相机(造影)、光学生物测量仪最受行业关注眼科医疗器械包括用于诊断和治疗眼科疾病
查看详情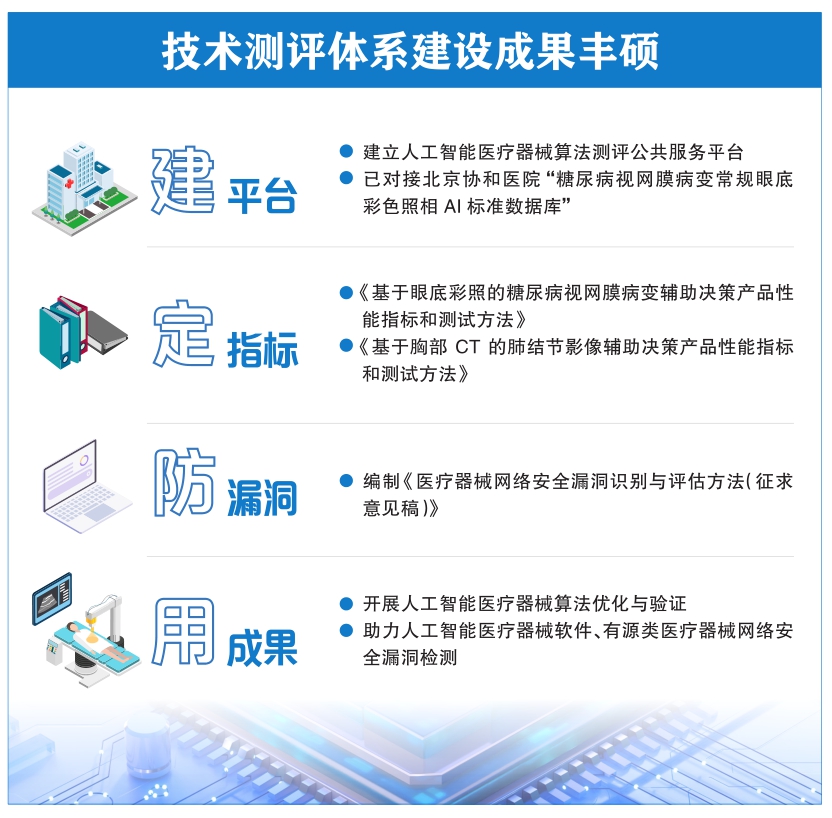
智能化医疗器械产品所属行业是一个强监管行业,产品安全有效性评价较谨慎。特别是以人工智能为代表的技术,本质上是基于海量数据驱动的黑盒算法,具有更新迭代快等特点,给监管
查看详情
测评技术研究工作组 测评技术研究工作组由中国信息通信研究院牵头组建,并作为组长单位组织开展人工智能医疗器械数据质控和产品验证等方面测评工作,研究数据质量要求及产品
查看详情
京、天津、辽宁、上海、江苏、浙江、山东、湖北、广东省(市)药品监督管理局,中检院(器械标管中心),器审中心,北京大学口腔医学院口腔医疗器械检测中心: 为贯彻国务院办公
查看详情
成都市双流区政府在2022年11月21日发布了“关于《双流区促进生物医药产业高质量发展的政策措施(征求意见稿)》公开征求意见的通知”,0人提出意见,也就是说这个
查看详情