24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

本指导原则旨在指导注册申请人对磁疗产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对磁疗产品的一般要求,申请人应依据
查看详情
本指导原则旨在指导注册申请人对医用内窥镜冷光源注册申报资料的准备及撰写,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用内窥镜冷光源的一般
查看详情
本指导原则旨在为技术审评部门审评凝血分析仪注册申报资料提供参考,同时也用于指导注册申请人对申报资料的准备及撰写。 本指导原则是对凝血分析仪的一般要求,注册申请
查看详情
本指导原则旨在指导注册申请人对空氧混合器产品注册申报资料的准备及撰写,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对空氧混合器产品的一般要求
查看详情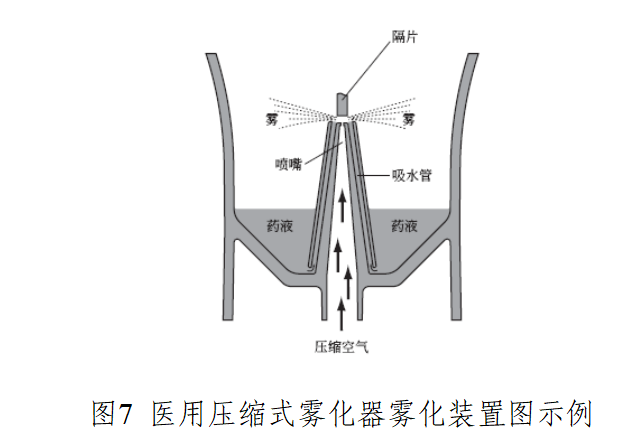
本指导原则旨在指导注册申请人提交医用雾化器的注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用雾化器的一般性要求,注册申请人应根
查看详情
本指导原则旨在指导注册申请人对半自动化学发光免疫分析仪注册申报资料的准备及撰写,同时也为技术审评部门审评提供参考。 本指导原则是对半自动化学发光免疫分析仪的
查看详情
高危经皮冠状动脉介入术(High-risk percutaneous coronary intervention,HR-PCI)患者主要指冠状动脉解剖/病变复杂且合并高危临床特征和(或)合并症,被冠状动脉旁路移植术(
查看详情
本指导原则旨在指导注册申请人对助听器注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。 本指导原则是对助听器的注册申报资料的一般要
查看详情