24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

8月26日,国家药监局发布创新医疗器械特别审查申请审查结果公示(2022年第6号),人乳头瘤病毒基因整合(14个型)核酸检测试剂盒(可逆末端终止测序法)等10项创新医疗器械特别审查申请获批,其中江浙沪地区5项高风险创新医疗器械特别审查申请获批。
查看详情
对于第一类医疗器械备案来说,近期法规调整较大,比如增加了检验报告的照片要求等,强化了备案资料真实性要求,及承诺制对企业的诚信行为监管要求。本文跟大家聊聊新《医疗器械生产监督管理办法》自2022年5月1日起施行后,第一类医疗器械若增加生产产品品种,应如何办理?
查看详情
依照法定程序,进行申请注册。 一类医疗器械注册申请材料: (一)境内医疗器械注册申请表; (二)医疗器械生产企业资格证明:营业执照副本; (三)适用的产品标准及说
查看详情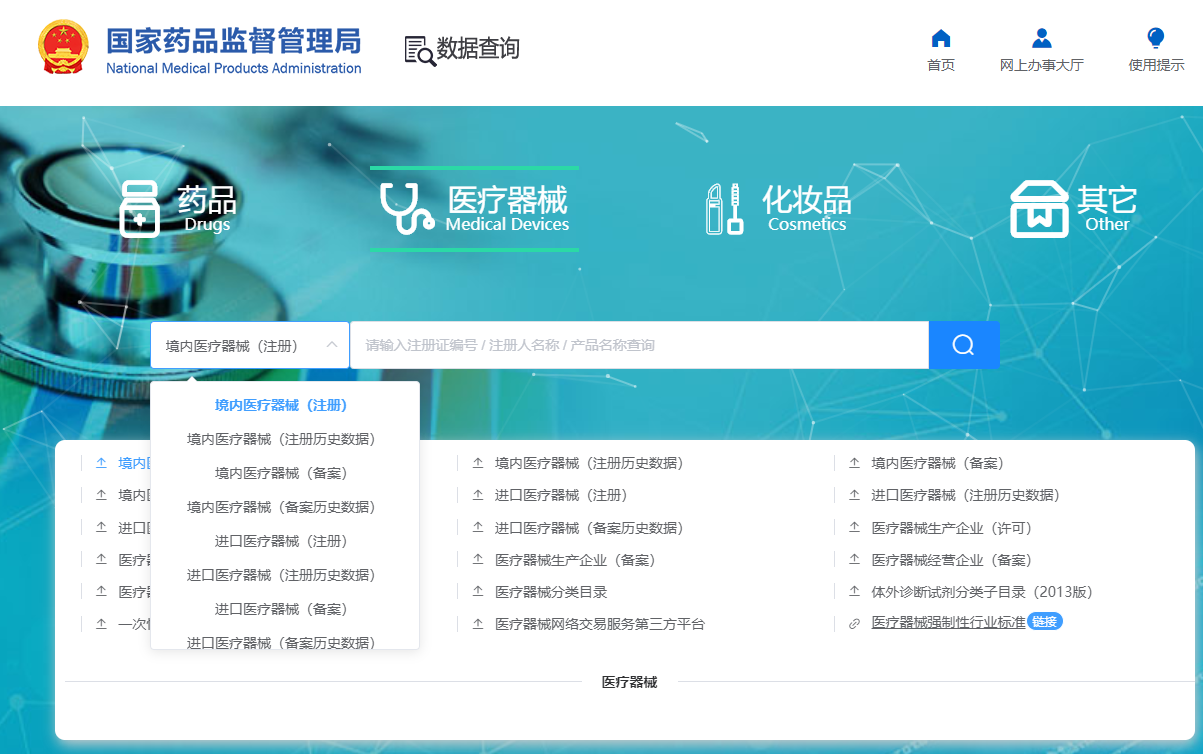
想知道您购买的医疗器械产品是否合法,就要查询产品是否拥有医疗器械注册证,那么医疗器械产品注册证怎么查询?接下来,和小编一起来看看吧!具体流程如下: 1、首先,我们打开
查看详情
体外诊断试剂和器械在国外统一称为体外诊断医疗器械。 属于医疗器械的一部分。在我国,体外诊断试剂是指:可单独使用或与仪器、器具、设备或系统组合使用, 在疾病的预防、
查看详情
一、政策法规类1. 中华人民共和国中央人民政府-行政法规库http://www.gov.cn/zhengce/index.htm 2. 国家药品监督管理局——医疗器械板块https://www.nmpa.gov.c
查看详情
一、 医疗器械生物学评价的策略与所含程序 该评价就是对XX公司所生产的YY产品进行的医疗器械生物学评价。所有YY产品采用同样的材料进行生产(若为系列产品)。 列出GB
查看详情
液相色谱串联质谱系统注册审查指导原则
本指导原则旨在指导注册申请人对液相色谱串联质谱系统注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考