24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

一次性使用人体动脉血样采集器 注册审查指导原则(征求意见稿)
本指导原则旨在帮助和指导注册申请人对一次性使用人体动脉血样采集器产品的注册申报资料进行准备,以满足技术

经皮肠营养导管注册审查指导原则 (征求意见稿)
本指导原则旨在帮助和指导注册申请人对经皮肠营养导管产品的注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审

近年来,药物支架(又称药物洗脱支架)在冠心病介入治疗中得到了广泛的应用,同时新的药物以及携带药物的技术也在不断的进入临床医生的视野。对于不同临床情况的患者以及不同
查看详情
在申请医疗器械注册时,需按《医疗器械注册管理办法》的要求提交一系列的注册申报资料,其中〈产品技术报告〉是对申请注册的医疗器械产品进行技术审评时具有重要参考价值的
查看详情
为全面证明药物支架这类高科技新产品的安全性和有效性特别是长期使用的安全性,应在良好完成上市前各项研究的基础上,积极开展以观察产品长期特性为重点的上市后临床研究。
查看详情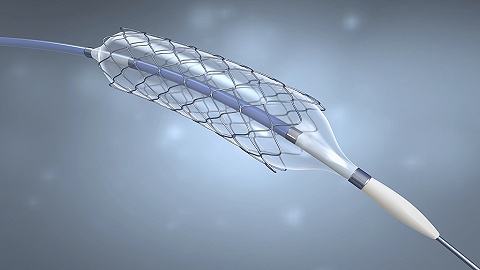
近几年,随着介入产品的创新,介入医学在国际上,包括我国,得到了迅速发展。它借助现代科学技术,如:超声、磁共振成像、CT、数字减影血管造影等,使医生在手术中能精确透视人体,将导管
查看详情
2021年11月,美国食品药品管理局(FDA)发布医疗器械软件功能申报指南草案(以下简称指南草案),公开征求意见,拟取代其2005年5月发布的医疗器械软件申报指南(以下简称2005版指
查看详情
提问:体外诊断试剂临床试验中对产品说明书的关注点有哪些?回答:体外诊断试剂临床实验设计和执行过程中应特别关注临床实验过程中的操作细节与相关产品说明书的一致性。无论是实
查看详情