24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

全国29个省、自治区、直辖市和部队医院已有671个机构完成了临床试验医疗器械机构备案工作。其中广东省、江苏省、北京市、上海市和浙江省临床试验机构备案数量位全国前五位,共完成备案260家医疗机构。
查看详情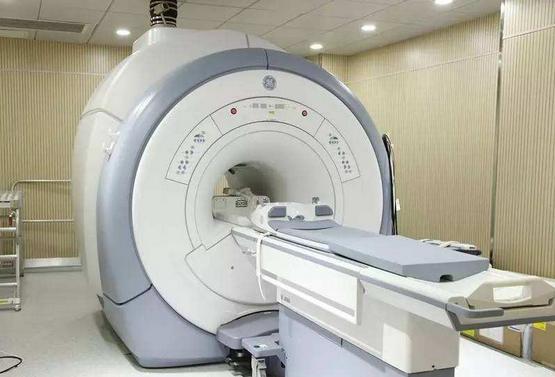
医用磁共振成像系统临床评价技术审查指导原则(2017年第6号)本指导原则是对医用磁共振成像系统临床评价的一般要求,注册申请人应依据具体产品的特性对医用磁共振成像系统临床评价的内容进行充实和细化。注册申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
查看详情
浙江省是医疗器械监管、审批最严格的地区之一,金华作为浙江省直辖市,医疗器械经营许可证/医疗器械经营备案凭证的办理与其它区域基本相同。新涉足行业人员在无专业机构/人员的辅导下,很难快速、高效的完成医疗器械经营许可证或医疗器械经营备案凭证的办理。飞速度在此为大家简要说明一下金华办理医疗器械经营许可延续程序。
查看详情
医疗器械经营许可证是医疗器械经营企业必须具备的证件,拥有此证件才能合法合规地销售医疗器械。很多企业老板都知道需要办理此资质,但是如何办理、办理过程中会遇到哪些问题都不甚清楚。不少老板会选择在网上找个中介公司办理,但是选择不靠谱的中介,会给您带来很大的麻烦。在此,飞速度先给大家梳理下医疗器械经营许可证的基础知识。
查看详情
2019年4月9日,广东省药品监督管理局网站发布《关于开展2019年第一期医疗器械临床试验监督抽查的通告》。
查看详情
本文着重介绍了医疗器械经营许可在办理地点、认证注意事项、以及医疗器械经营许可办证等级方面进行大量详细的说明,这里希望大家注意的是,内容方面有很多地方还介绍的不够完善,有些点还没有补充完整,希望后续大家能够提出相对应的建议。
查看详情
第三类医疗器械经营许可证即将到期,错过延期时机将导致医疗器械经营许可证失效。企业如何办理经营许可证的延期?以及延期办理与首次办理存在哪些差异?飞速度为您解答。
查看详情
相比于药物临床试验领域有很多成熟经验可以学习、参照,医疗器械临床试验领域还处于起步、探索阶段。临床试验设计及医疗器械临床试验方案对临床评价的合规合法性至关重要,飞速度为您提供医疗器械临床试验方案范本供您参考。
查看详情