24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

青光眼是一种具有视乳头萎缩及凹陷、视野缺损及视力下降等特征的疾病。患者因眼球内房水循环受阻引起眼压升高,并超过视神经所能耐受的眼压限度,从而导致视神经慢性损伤。
查看详情
7月1日,中国食品药品检定研究院(以下简称中检院)牵头的电气电子工程师学会(IEEE)人工智能医疗器械标准工作组起草的IEEE 2801—2022(医学人工智能数据集质量管理推
查看详情
2022年7月,国家药品监督管理局共批准注册医疗器械产品197个。其中,境内第三类医疗器械产品152个,进口第三类医疗器械产品20个,进口第二类医疗器械产品22个,港澳台医疗器械产
查看详情
8月17日,国家药监局网站发布《关于政协第十三届全国委员会第五次会议第04104号(医疗卫生类383号)提案答复的函》。对于委员提出的《关于进一步完善第二类医疗器械注册技术审评
查看详情
新修订《医疗器械临床试验质量管理规范》已于5月1日施行。随着医疗器械临床试验相关法规的陆续出台完善,省级层面医疗器械监管工作面临新形势、新要求,如何建立一支与省级
查看详情
近日,Galien 基金会宣布了 2022 年 Prix Galien USA 奖项最佳医疗器械创新提名人选,BD、波士顿科学、奥林巴斯、博士伦...盖伦奖(Prix Galien Award)评选标准一如既往,提名者必须
查看详情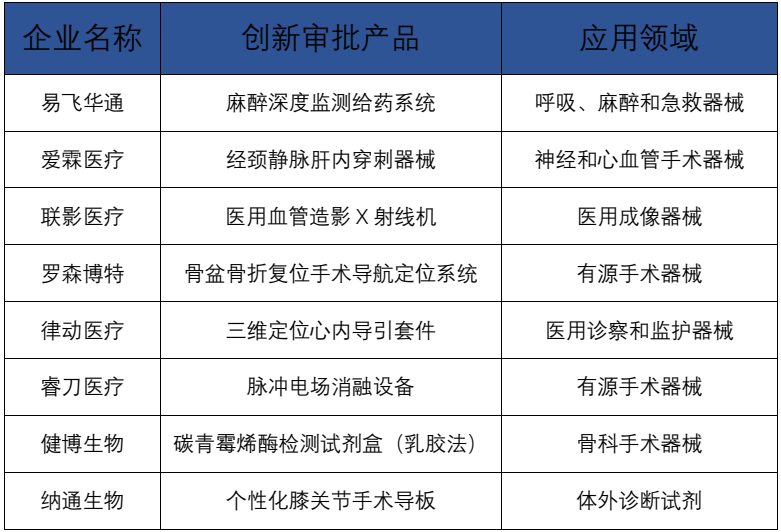
7月份已有8个产品进入创新审批通道,涵盖手术机器人、诊断试剂、手术器械等领域;6个创新医疗器械获批上市,涵盖肠息肉诊疗、植入式左心室辅助系统等领域。 这些进入创新
查看详情
国家药监局批准人类辅助生殖技术用医疗器械标准化技术归口单位换届,现予公布(组成方案见附件)。 特此公告。 附件:人类辅助生殖技术用医疗器械标准化技术归口单位组成
查看详情