24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

口腔印模材料注册审查指导原则
本指导原则旨在指导注册申请人准备及撰写口腔印模材料产品注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则

有创血压监护产品注册审查指导原则
本指导原则旨在指导申请人对有创血压监护产品(以下简称“产品”)注册申报资料的准备及撰写,同时也为技术审评部门审评注册

一次性使用无菌阴道扩张器注册审查指导原则 本指导原则旨在帮助和指导申请人对一次性使用无菌阴道扩张器(以下简称扩张器)注册申报资料的准备及撰写,同时也为技术审评部门
查看详情
一次性使用子宫颈球囊扩张导管注册审查指导原则
本指导原则旨在指导和规范一次性使用子宫颈球囊扩张导管产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、

经鼻肠营养导管注册审查指导原则 本指导原则旨在指导注册申请人对经鼻肠营养导管注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对经鼻肠营养
查看详情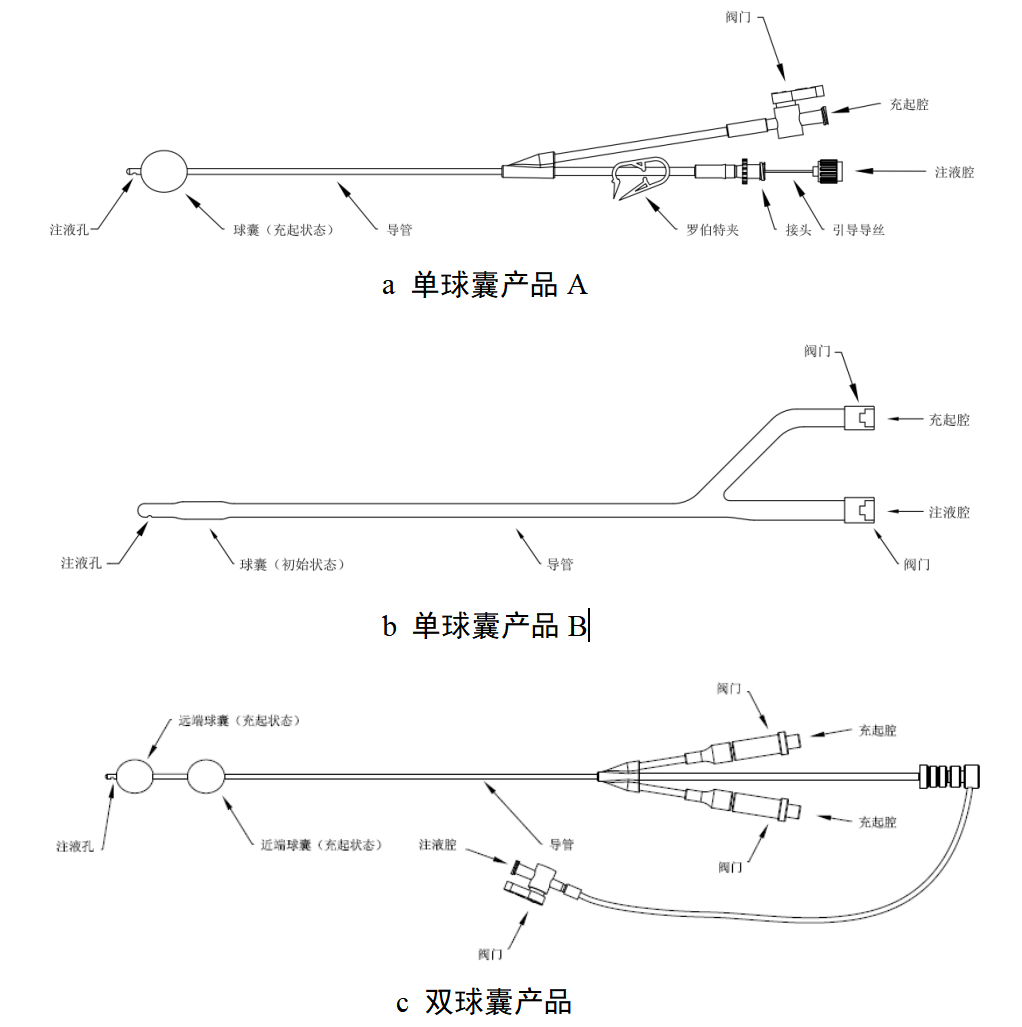
子宫输卵管造影球囊导管注册审查指导原则 本指导原则旨在指导注册申请人对子宫输卵管造影球囊导管注册申报的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是
查看详情
病原体特异性M型免疫球蛋白定性检测试剂注册审查指导原则 (2022年修订版征求意见稿)
本指导原则旨在指导注册申请人对病原体特异性M型免疫球蛋白(Immunoglobulin M,IgM)定
弓形虫、风疹病毒、巨细胞病毒、单纯疱疹病毒抗体及G型免疫球蛋白抗体亲合力检测试剂注册审查指导原则(2022年修订版征求意见稿)
本指导原则旨在指导注册申请人对弓形虫、