24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
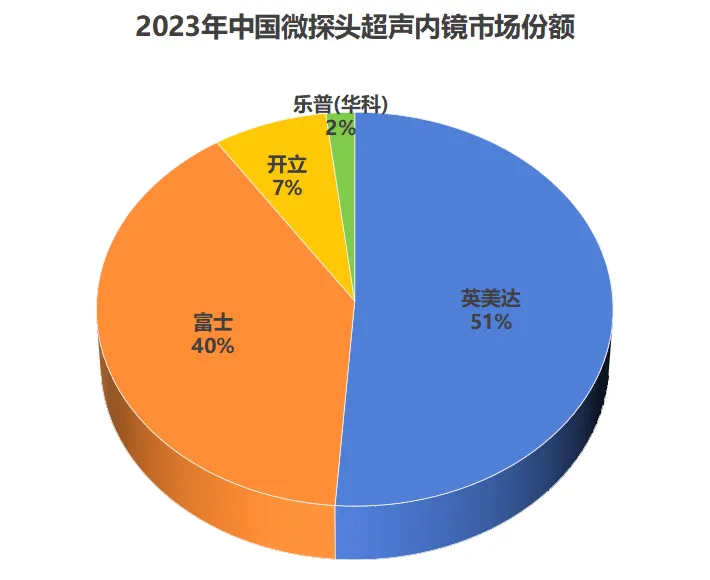
超声内镜(endoscopic ultrasonography, EUS)是将内镜与超声完美结合的一项技术,被称为内镜医生的“第三只眼”,它融合了“内镜”和“超声&rdquo
查看详情
受理号 企业名称 产品名称 生产地址 核查结论 结论日期 CQZ2400326 深圳市家鸿口腔医疗股份有限公司 个性化匹配式基台及螺钉 深圳市龙华区观
查看详情
高压灭菌器作为医疗、科研和工业领域中不可或缺的设备,承担着确保物品无菌状态的重任。其高效灭菌能力的背后,是对设备精心维护与规范操作的严格要求。本文将全面解析高压灭菌
查看详情
在医疗和科研领域,高压灭菌器作为一项不可或缺的技术装备,扮演着守护无菌环境、预防交叉感染的重要角色。它的存在,不仅确保了医疗器械、实验室用品的无菌状态,还为生物安全、疫
查看详情
在康复医学领域,牵引带作为一种非侵入性治疗工具,广泛应用于各类骨科和神经科疾病的治疗与康复过程中。它以其独特的治疗机制和广泛的适应症,成为医生和患者青睐的辅助疗法之一
查看详情
在有源医疗器械领域,内置充电电池的应用日益广泛,尤其是在便携式和移动式设备中,以确保设备的持续可用性和操作灵活性。GB 9706.1-2020作为医疗电气设备安全的基本标准,对内
查看详情
在医疗器械产业蓬勃发展的今天,北京市医疗器械注册人制度的实施,为行业内的企业提供了创新和合作的新机遇。尤其在二类医疗器械领域,如体外诊断试剂的开发与生产,这一制度更
查看详情
在现代医疗体系中,大型医用设备不仅是医疗机构的核心资产,更是提升诊疗水平、保障患者健康的关键工具。然而,由于这类设备的特殊性——技术复杂、资金投入巨大、
查看详情