24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
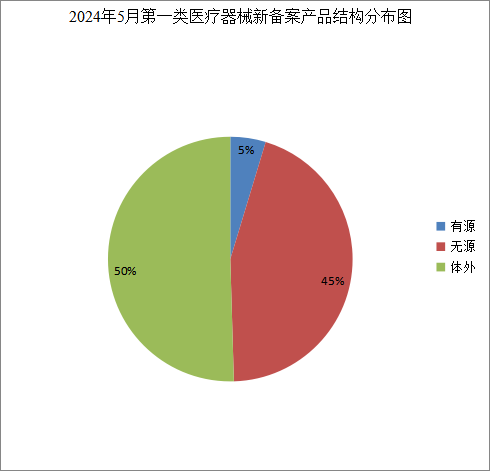
2024年5月,浙江省内各市市场监督管理局共新备案第一类医疗器械产品214个,其中有源类10个,无源类96个,体外诊断试剂108个(具体产品见附件)。 按照备案人所在辖区分析,杭州
查看详情
医疗领域消费新增长点公布:前沿技术融合、社会办医、银发经济......01、国家明确医疗新消费场景 脑机接口、数字孪生被点名 近日,国家发改委、商务部等5部门联合印发《
查看详情
为加强医疗器械监督管理,保障医疗器械产品质量安全有效,国家药品监督管理局组织对半导体激光治疗机、医用脉搏血氧仪、正畸丝3个品种进行了产品质量监督抽检,有7批(台)产品
查看详情
发光测定仪是一种在生物学、医学、环境科学等领域广泛应用的分析仪器,它主要用于检测和定量分析生物样本中特定物质的浓度。发光测定仪的工作原理是基于化学发光或生物发
查看详情
在糖尿病管理的前沿,持续葡萄糖监测系统(Continuous Glucose Monitoring System,简称CGMS)已成为不可或缺的工具。CGMS通过实时监测患者体内的葡萄糖水平,提供连续的数据流
查看详情
在现代神经外科领域,脑积水分流器作为一种关键的治疗手段,广泛应用于脑积水的治疗中。然而,随着医疗影像技术的发展,尤其是磁共振成像(MRI)的普及,磁场对脑积水分流器的安全
查看详情
在医疗器械领域,脑积水分流器作为治疗脑积水的关键设备,其注册单元划分是确保产品安全性和有效性的重要环节。鉴于脑积水分流器的多样性和复杂性,科学合理地进行注册单元划
查看详情
在新药研发的漫长旅程中,药物临床试验是连接实验室研究与市场应用的关键桥梁。根据新版《药品注册管理办法》,临床试验被精细划分为I、II、III、IV期,每期试验都承载着独特
查看详情