24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

结核分枝杆菌复合群耐药基因突变检测试剂注册技术审查指导原则(2017年第25号)本指导原则旨在指导注册申请人对结核分枝杆菌复合群耐药基因突变检测试剂注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。本指导原则是针对结核分枝杆菌复合群耐药基因突变检测试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需阐述具体理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
由于应急审批的特殊性,通过应急审批获批的医疗器械注册证有效期较短,有效期通常是3个月、6个月或1年,注册证到期后自动失效,部分省份要求重新提交注册申报,那么注册证到期后,已经具备医疗器械生产体系的企业该如何正式迈入医疗器械行业,获得一张真正的“5年有效期注册证”?
查看详情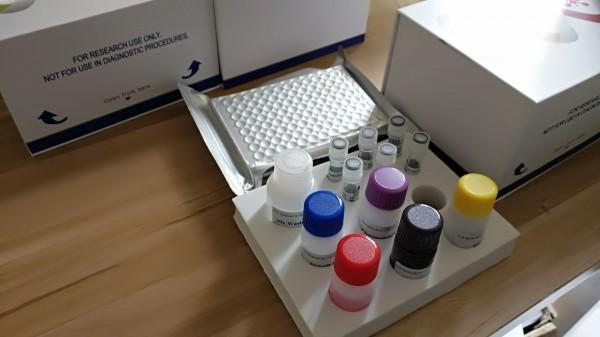
人红细胞反定型试剂注册技术审查指导原则(2016年第131号)本指导原则旨在指导注册申请人对人红细胞反定型试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对人红细胞反定型试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情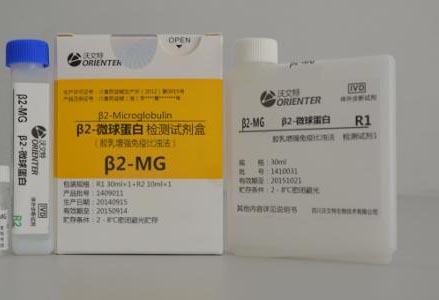
β2-微球蛋白检测试剂盒(胶乳增强免疫比浊法)注册技术审查指导原则(2016年第29号)本指导原则旨在指导注册申请人对β2-微球蛋白(β2-Microglobulin,β2-MG)检测试剂盒(胶乳增强免疫比浊法)注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对β2-微球蛋白检测试剂盒(胶乳增强免疫比浊法)的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
2020年2月,国家药品监督管理局共批准医疗器械注册产品170个。其中,境内第三类医疗器械产品118个,进口第三类医疗器械注册产品16个,进口第二类医疗器械注册产品32个,港澳台医疗器械注册产品4个。
查看详情
补发浙江省药品监督管理局2020年3月18日的一个重要通知,关于公布第二类医疗器械检验机构的公告,浙江省内国家认证认可监督管理委员会认定且有相关医疗器械承检范围的检验机构增加到7家。
查看详情
近日,欧盟委员会在欧洲官方杂志(Official Journal of the EuropeanUnion)发布了疫情期间针对医疗器械和个人防护用品的符合性评价和市场监督程序的建议,开启防疫用医疗器械和个人防护装备进入欧盟的绿色通道。
查看详情
近日,药监总局出台2020年医疗器械行业标准制修订计划,86项新标准将制订,可能影响医疗器械注册、医疗器械经营许可事项、医疗器械临床试验事项,一起来了解。
查看详情