24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

中药新药临床研究指导原则(1993第一辑)由中华人民共和国卫生部指定发布的:前言
为促进中药新药临床研究的科学化、标准化和规范化,提高中药新药的研制水平,我部曾于1987年
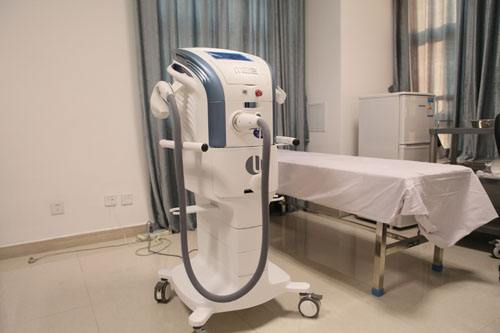
强脉冲光治疗仪注册技术审查指导原则(2016年第21号),本指导原则旨在指导注册申请人对强脉冲光治疗仪注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情
脉搏血氧仪设备临床评价技术指导原则(2016年第21号),本指导原则旨在指导注册申请人对脉搏血氧仪设备(以下简称血氧仪)临床评价资料的准备及撰写,同时也为技术审评部门审评血氧仪临床评价资料提供参考。本指导原则是对血氧仪临床评价的一般性要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对临床评价资料的内容进行充实和细化。
查看详情
医用X射线诊断设备(第三类)注册技术审查指导原则(2016年修订版)(2016年第21号),本指导原则旨在指导注册申请人对医用X射线诊断设备(第三类)注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情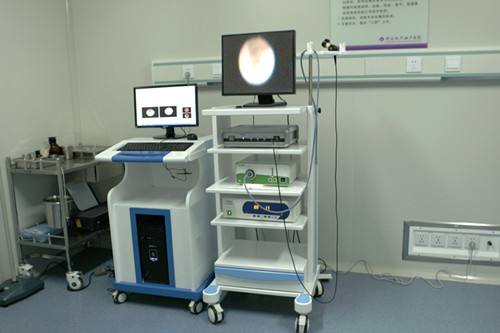
第二类腹腔镜手术器械产品注册技术审查指导原则(2017年第30号),本指导原则旨在指导和规范第二类腹腔镜手术器械的技术审评工作,帮助审评人员理解和掌握该类产品结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。
查看详情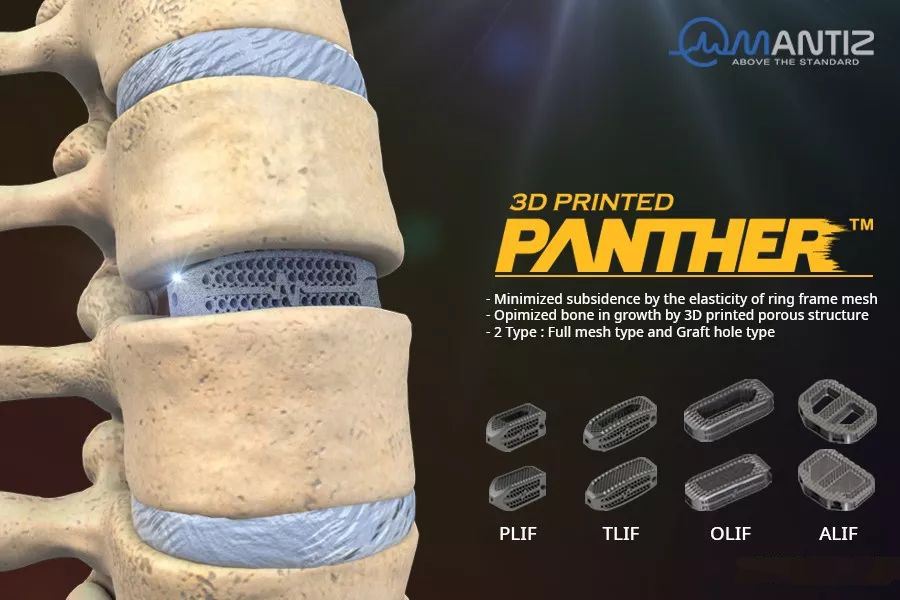
脊柱植入物临床评价质量控制注册技术审查指导原则(2020年31号),本指导原则是对注册申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他技术论证方法,也可以采用,但是需要提供详细的研究资料和论证资料。企业应在遵循相关法规和技术标准的前提下使用本指导原则。
查看详情
辅助生殖用穿刺取卵针注册技术审查指导原则(2020年第31号),本指导原则旨在为注册申请人进行辅助生殖用穿刺取卵针类医疗器械产品注册申报提供参考,同时也为审评机构对注册申报资料的技术审评提供技术指导。
查看详情
水胶体敷料产品注册技术审查指导原则(2020年第31号),本指导原则旨在指导水胶体敷料产品的研究开发、产品注册申报资料撰写和技术审评。本指导原则是对水胶体敷料产品的一般要求,注册申请人应依据具体产品的特性对注册申报资料的内容进行充分说明和细化。注册申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需详细阐述理由及相应的科学依据。
查看详情