24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

北京市食品药品监督管理局
填 表 说 明
1.按照《医疗器械注册管理办法》《体外诊断试剂注册管理办法》及相关文件的规定报送资料。
2.本申请表应打印。填写内容应

北京市食品药品监督管理局
填 表 说 明
1.按照《医疗器械注册管理办法》《体外诊断试剂注册管理办法》及相关文件的规定报送资料。
2.本申请表应打印。填写内容应
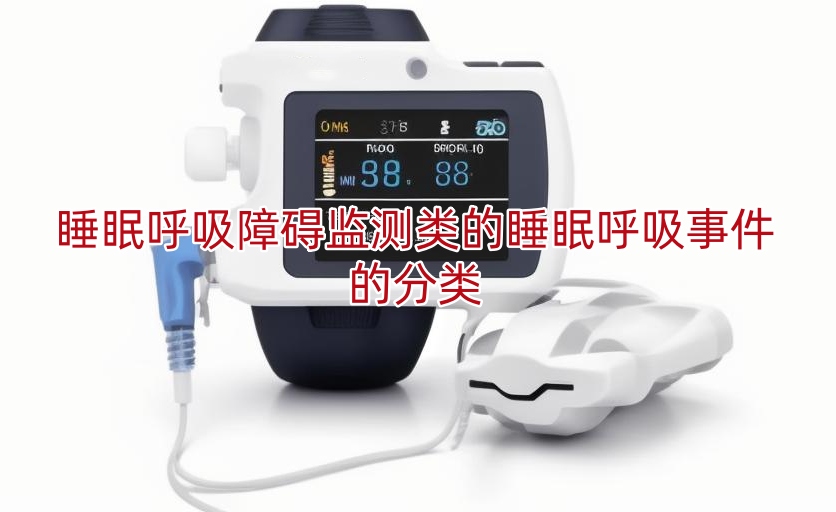
睡眠呼吸障碍是一种常见的睡眠相关疾病,影响着全球数百万人口的健康与生活质量。睡眠呼吸监测设备作为诊断和监测这类障碍的关键工具,其准确识别和分类睡眠呼吸事件的能力,对于
查看详情
在医疗器械行业,产品的稳定性验证是确保其在声明的有效期内维持安全性和有效性的重要环节。有效期验证不仅考验着产品的内在质量,还考量着其对外界环境的适应能力,尤其是运
查看详情
在医疗器械行业,产品注册不仅是企业进入市场的通行证,更是产品质量与安全性的官方认证。尤其在涉及委托生产的情况下,注册质量管理体系核查成为确保产品合规性的关键环节。本文
查看详情
在医疗科技领域,特别是体外诊断试剂的开发过程中,企业间的合作模式日益多样化,其中母子公司之间的协作成为一种常见的实践。当全资子公司负责产品的初始研发,而母公司则承担
查看详情
发光测定仪是一种在生物学、医学、环境科学等领域广泛应用的分析仪器,它主要用于检测和定量分析生物样本中特定物质的浓度。发光测定仪的工作原理是基于化学发光或生物发
查看详情
在糖尿病管理的前沿,持续葡萄糖监测系统(Continuous Glucose Monitoring System,简称CGMS)已成为不可或缺的工具。CGMS通过实时监测患者体内的葡萄糖水平,提供连续的数据流
查看详情