24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

本指导原则旨在指导注册申请人(以下简称申请人)对脱细胞基质软组织创面修复材料产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则系对脱细胞
查看详情
3月19日,《中国医药报》法治天地版刊发了《某自建网站销售“消字号”隐形眼镜护理液,应如何处理?》一文,涉案的隐形眼镜护理液仅标示了生产企业卫生许可证号,并
查看详情
本指导原则旨在指导注册申请人对高分子合成可吸收外科缝线开展同品种临床评价,同时也为技术审评部门审评可吸收外科缝线同品种临床评价资料提供参考。 本指导原则是对
查看详情
1、年度检查概况 2023年度,上海市器审中心依据《医疗器械生产质量管理规范》和《医疗器械生产质量管理规范附录植入性医疗器械》对植入性医疗器械企业依申请开展现场核查,
查看详情
1、年度检查概况 2023年度,本市无菌医疗器械现场核查合计发现缺陷1666项。厂房与设施(178项次)、设备(100项次)、设计开发(282项次)、采购(213项次)、生产管理(399项次)、
查看详情
1、年度检查概况 2023年度,本市定制式义齿现场核查合计发现缺陷409项。厂房与设施(22项次)、设备(29项次)、文件管理(34项次)、采购(24项次)、生产管理(97项次)、质量控制
查看详情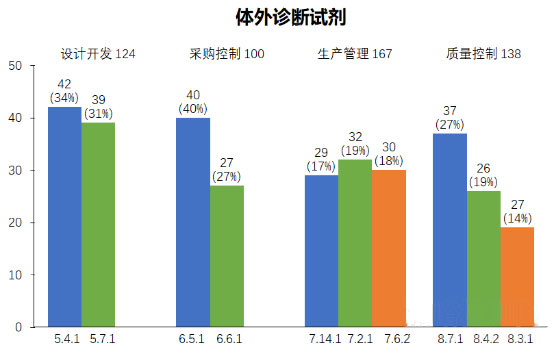
1、年度检查概况 2023年度,上海市器审中心依据《医疗器械生产质量管理规范》和《医疗器械生产质量管理规范附录体外诊断试剂》对体外诊断试剂企业依申请开展现场核查,合计
查看详情
角膜地形图系统,作为一种精密的眼科检测设备,通过绘制角膜表面的三维图像,为医生提供角膜形态的详细分析数据,对角膜疾病的诊断、手术规划、术后监测、隐形眼镜适配等方面发
查看详情