24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

想象一下,你正把一款进口玻尿酸填充剂引进中国市场,包装上印着“适用于面部塑形”,但境外原厂文件只写了“用于真皮层注射”——这种细微差
查看详情
2025年5月,山东省药品监督管理局共批准注册第二类医疗器械产品51个(具体产品见附件)。 特此公告。 附件:2025年5月批准注册医疗器械产品目录2025年5月批准注册医疗
查看详情
山东省药品监管数字化改革迎来重大突破!近日,山东省药监局正式宣布,自6月1日起,国产第二类医疗器械注册、体外诊断试剂审批、医疗机构制剂注册、药品及医疗器械广告审查等
查看详情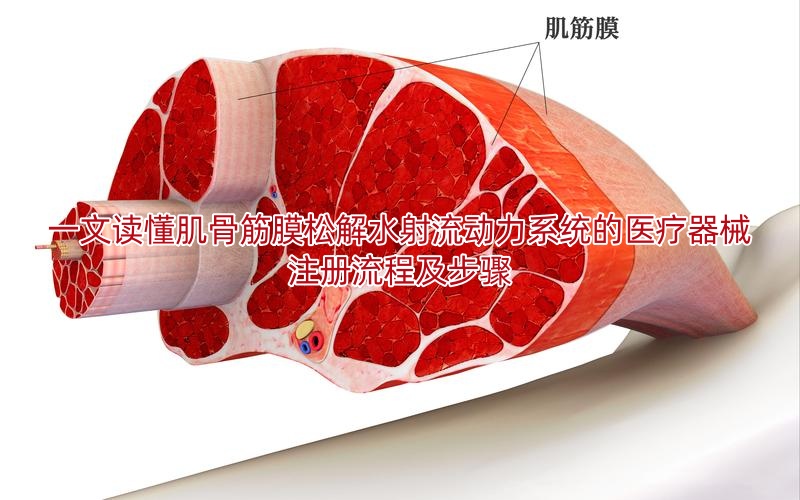
第一步:明确产品分类与监管路径 肌骨筋膜松解水射流动力系统因具备组织切割与药物输注双重功能,需重点厘清监管逻辑: 1.核心分类依据: 水射流切割功能(工作
查看详情
一、《公告》的起草背景? 党中央、国务院高度重视药品医疗器械质量安全。药品医疗器械是重要的健康产品,具有信赖品的特征,群众难以在消费前和消费中通过一般识别了解其质
查看详情
为进一步发挥药品医疗器械产业链质量安全内部监督作用,及时发现和控制药品医疗器械安全风险,根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《医疗器械监
查看详情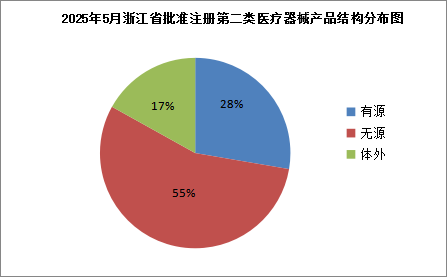
2025年5月,浙江省药品监督管理局共批准注册第二类医疗器械产品65个,其中有源类18个,无源类36个,体外诊断试剂11个(具体产品见附件)。 按照注册申请人所在辖区分析,批准注
查看详情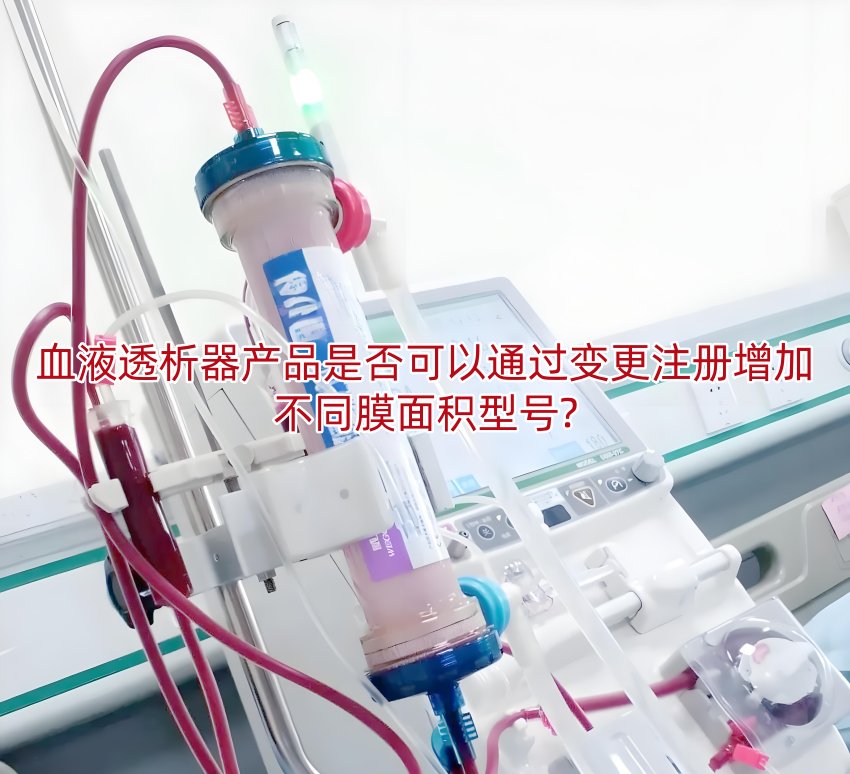
如果你是生产血液透析器的企业,想给现有产品增加1.5㎡、2.0㎡等不同膜面积的新型号,却纠结“要不要重新注册”“检测怎么做”,别慌——药监
查看详情