24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

2025年5月,河南省药品监督管理局共批准注册第二类医疗器械产品95个,具体产品详见附件。 特此公告。 附件:2025年5月批准注册医疗器械产品目录 2025年6月6日2025年
查看详情
一、目的 为指导二代基因测序相关体外诊断试剂管理属性和管理类别判定,根据《医疗器械监督管理条例》《体外诊断试剂注册与备案管理办法》《体外诊断试剂分类规则》《体
查看详情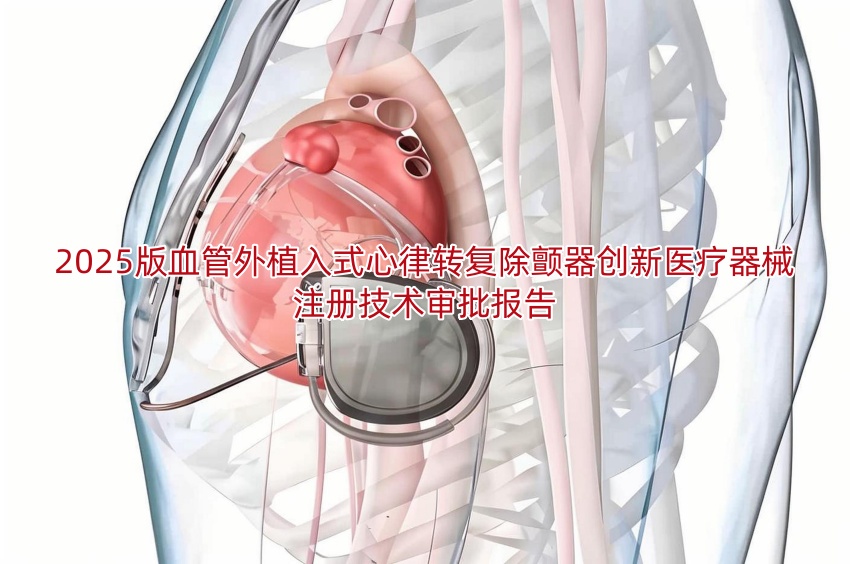
当心脏突然陷入致命性室颤,传统除颤器需要将电极穿入血管直抵心脏——这个画面即将成为历史。2025年,美敦力公司研发的“血管外植入式心律转复除颤器&rdqu
查看详情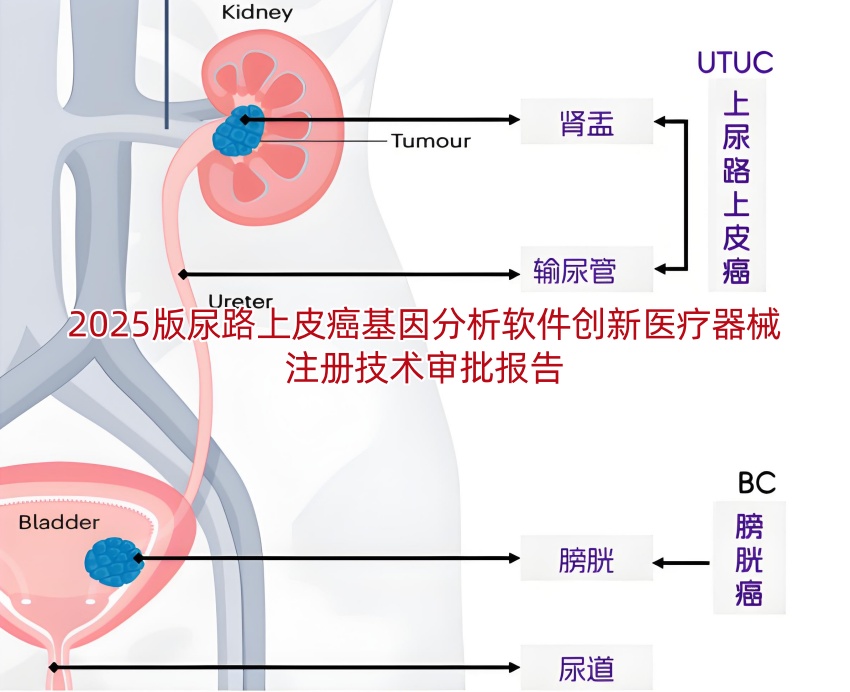
膀胱镜检查是诊断尿路上皮癌的金标准,但作为侵入性操作常令患者望而生畏。2025年,一款名为“Canhelp-UriBLAD”的基因分析软件通过国家药监局创新审批(注册证号
查看详情
想象一下,你是一家社区诊所的负责人。某天药监执法人员突击检查,在处置室的角落翻出三盒过期半年的缝合线。你辩解“这些早就不用了”,但执法人员指着混放在有效
查看详情
欧盟成员国6月2日通过一项决议,将限制中国医疗器械企业参与欧盟公共采购项目。根据新规,未来五年内,中国制造商将被排除在金额超过500万欧元的欧盟医疗器械公共招标之外。
查看详情
为了进一步规范软组织再生型疝修补补片(以下简称为“再生型疝补片”)动物试验,并指导该类产品注册申请人进行动物试验设计及注册资料准备,制定本审评要点。
查看详情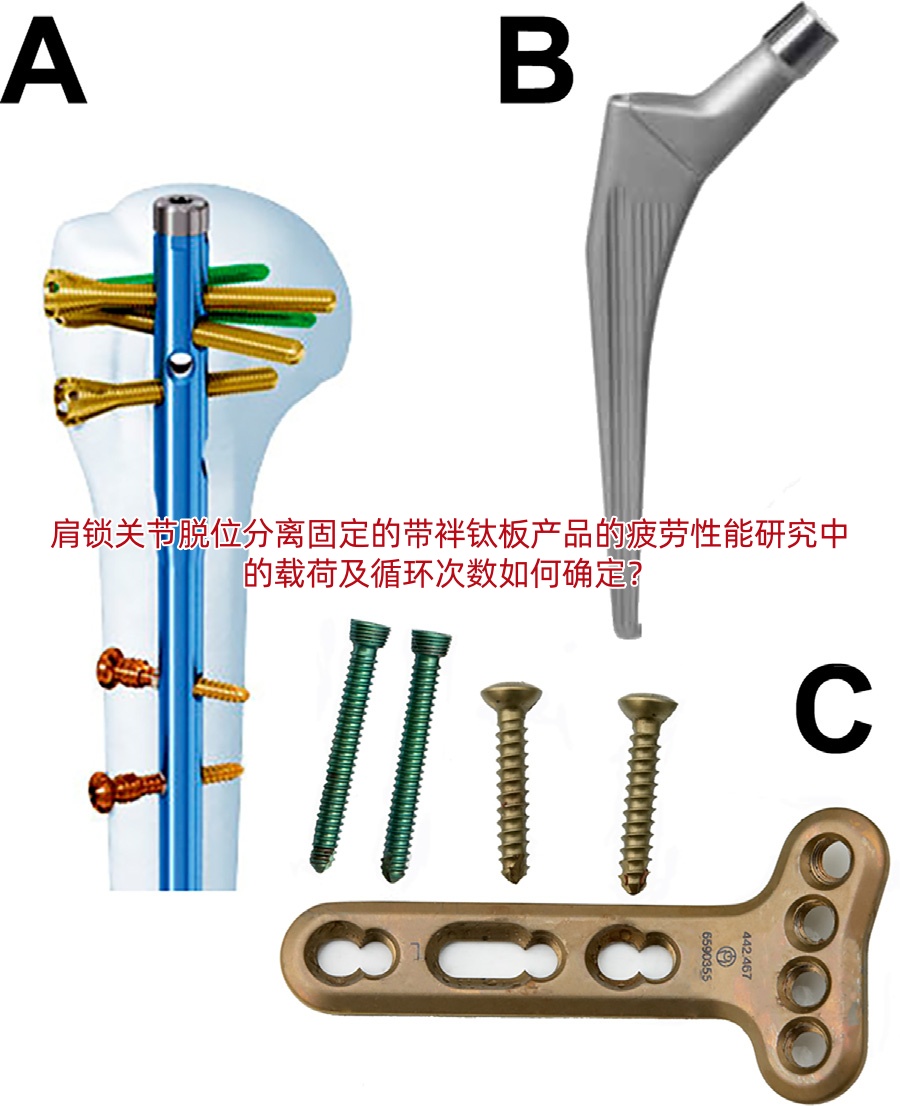
如果你是生产骨科固定带袢钛板的企业,正为肩锁关节脱位或下胫腓联合分离产品做疲劳性能测试,却被“载荷怎么定”“循环次数算多少”卡住申报进度&mda
查看详情