24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

体外诊断试剂行业是一个有技术门槛的行业,对于体外诊断试剂注册?企业来说,生物技术专业知识能力是要素之一。第三方医药技术咨询公司或者咨询老师更多的是带教、是培养,即使聘请了第三方,企业仍然需要具有专业知识的人员。
查看详情
猴痘病毒核酸检测试剂技术审评要点(试行)
本审评要点旨在指导注册申请人对猴痘病毒核酸检测试剂注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本审

今年6月,国家药监局就《医疗器械经营质量管理规范附录:第三方物流质量管理(征求意见稿)》(以下简称《征求意见稿》)向社会公开征求意见,以进一步强化医疗器械第三方物流的
查看详情
我国规定,医疗器械注册申请人/注册人需确定产品的使用期限。如何确定医疗器械的使用期限?国家药品监督管理局发布了《有源医疗器械使用期限注册技术审查指导原则》,给出了
查看详情
无源医疗器械敷料、植入类汇总
1、可吸收组织密封膜
用于胸外科手术中的漏气、外科手术中软组织的低压渗漏或缓慢出血或液体渗漏的密封或加强。2、 无细胞真皮基质采用猪皮

医疗器械临床试验是医疗器械研发注册环节中至关重要的部,同时,临床试验机构的数量变化在一定程度上也体现了当地医疗器械临床实验质量管理水平。 2017年11月发布的《医
查看详情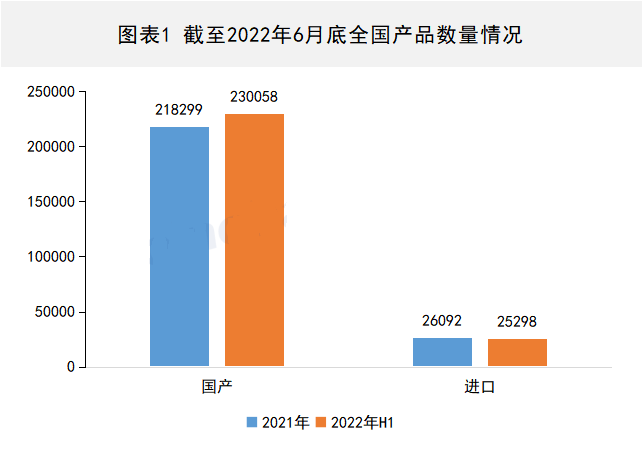
总体情况 截至2022年6月底,全国医疗器械产品有效注册、备案数达255356件,较2021年底增长4.49%,其中国产产品有230897件,进口产品有218299件,国产产品占比90.42%。产品新增动态
查看详情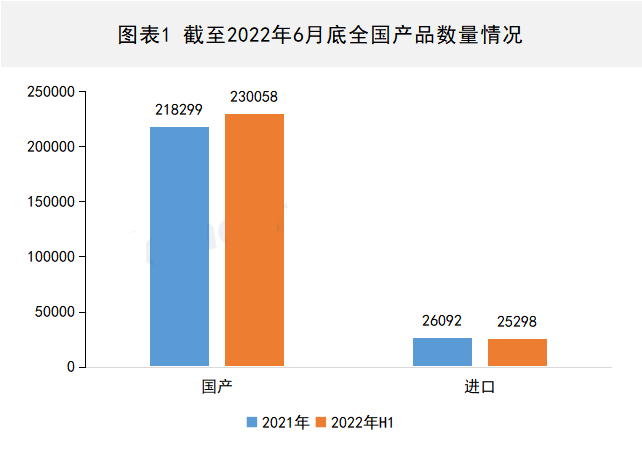
总体情况截至2022年6月底,全国医疗器械产品有效注册、备案数达255356件,较2021年底增长4.49%,其中国产产品有230058件,进口产品有25298件,国产产品占比90.09%。产品新增动态1、
查看详情