24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
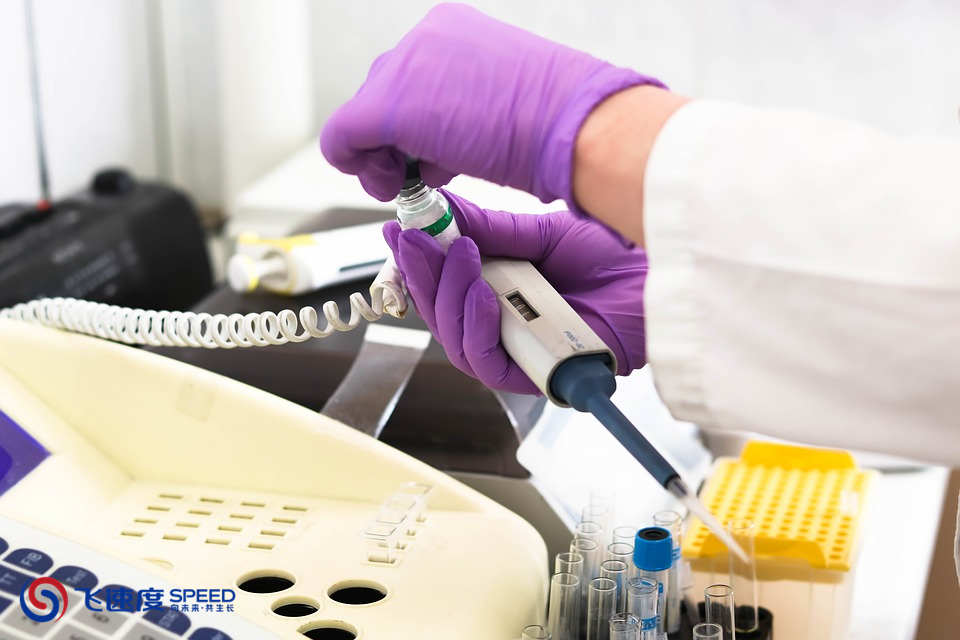
进口医疗器械注册与国产医疗器械注册既有区别又有相同点,关于进口医疗器械注册是否需要检验,检验的要求与国产医疗器械注册检验有无差异,在哪来检验,本文为您介绍。
查看详情
又到了CMDE疑难解答时间,本期解答的是超声刀&灌流器产品使用疑难,一起来看看!在超声软组织切割止血设备的动物实验中,如何选择有代表性的超声切割头型号?动物实验中超声切割头代表性模型的选择应参照《超声软组织切割止血系统注册技术审查指导原则
查看详情
医疗器械的生物评价对于保障医疗器械的安全性有着重要的作用,尤其是免于临床试验的产品和与同品种比较后获准进入国内市场的产品。一般来说,与人体直接或间接接触的医疗器械(包括患者和医务人员)应进行合理、全面的评估,以确定其与人体接触所造成的生物风险是否可接受。
查看详情
11月2日,国家药品监督管理局医疗器械技术审评中心发布通知,就《医疗器械中应用的纳米材料安全性和有效性评价框架指导原则(征求意见稿)》(以下简称《征求意见稿》)公开征求意见。该指导原则将规范产品技术审评,指导企业进行应用纳米材料的医疗器械产品注册申报。
查看详情
医疗器械注册证号是医疗器械的“身份证”。熟悉医疗器械注册号的相关含义,对于辨别医疗器械是否合法具有重要意义。 对于个别非法厂商将医疗器械销售至非应用范围的非法行为,国家食品药品监督管理局及卫生执法部门将依法追究法律责任。
为方便大众对医疗器械注册证号的识别,依据2014年《医疗器械注册管理办法(局令第4号)》规定,特做出以下解析:
接触镜及其护理产品是眼科重要器械,常见的接触镜护理产品包括日常护理产品、清洁产品、舒润产品、冲洗产品,随着接触镜越来越广泛的运营,接触镜护理产品申请医疗器械注册?的也随之增多,逐渐形成一个有巨头参与又各有特色的不大不小的市场。
查看详情
医疗器械临床试验常常会碰到过程中临床试验方案修改的情形,那么在医疗器械注册资料提交时,是否需要提交历次版本医疗器械临床试验方案呢?且看总局官方解答。
查看详情
目前全球新型冠状病毒肺炎(COVID-19)疫情防治工作进入攻坚阶段,重型、危重型患者的有效救治是降低病死率的关键。人工肝血液净化系统可以清除炎症因子,减轻炎症反应对机体的损伤,对重型、危重型患者的救治具有重要临床意义。
查看详情