24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
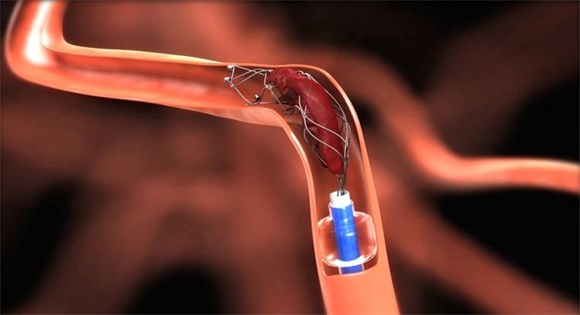
近日,器审中心(CMDE)连续公开了多个三类医疗器械产品技术审评报告,其中包含由医科达(英国)有限公司 Elekta Limited 提供的进口三类医疗器械磁共振引导放射治疗系统注册技术审评报告,为同类产品注册了解审评老师审核重点提供依据,也为注册人员准备该产品注册资料提供完美模板。本期分享的注册技术审评报告是由珠海通桥医疗科技有限公司研发的三类医疗器械取栓支架,该产品由一个自扩张的取栓支架、输送丝、支撑弹簧圈、显影弹簧圈、热缩套管、显影环和保护鞘管组成。其中取栓支架和输送丝均选用镍钛合金材料制成,显影环材质为铂铱合金,显影弹簧圈材质为铂钨合金。取栓支架用于在患者缺血性卒中发作8小时内移除堵塞在颅内大动脉血管内的血栓以达到恢复血流的治疗目的,包括颈内动脉、大脑中动脉的M1和M2段、大脑前动脉的A1和A2段。
查看详情
为提升医疗器械审评公开透明度,器审中心于近期公开医疗器械产品技术审评报告。本期的注册技术审评报告是由医科达(英国)有限公司 Elekta Limited 提供的进口三类医疗器械磁共振引导放射治疗系统(MRI guided radiotherapy system),该产品将超导磁共振成像系统(以下简称 MR)和安装在滑环机架上的驻波直线加速器集成为一体,实现了在患者治疗位置 进行磁共振成像的功能,治疗时系统可根据肿瘤的解剖结构调整剂量分布,最大可能地保护正常组织;同时可以在X射束治疗肿瘤时实时采集磁共振图像监测肿瘤位置。一起来看看磁共振引导放射治疗系统注册审评老师关注的重点在哪?
查看详情
近日,润方(长春)生物科技有限公司(以下简称“润方生物”)获得了由省药监局颁发的第二类医疗器械生产许可证,成为省内首个按医疗器械注册人制度试点获批上市的第二类医疗器械生产企业,打破了此前医械产品注册和生产许可“捆绑”模式。
查看详情
在《中国(江苏)自由贸易试验区苏州片区建设实施方案》中,园区将“开展医疗器械上市许可持有人制度试点,鼓励苏州片区医疗器械注册人委托区外医疗器械生产企业生产产品”作为一项重点制度创新推进。首个医疗器械注册人制度试点产品获批,意味着该创新制度正式落地。
查看详情
为贯彻落实中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)和河南省人民政府办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的实施意见》(豫政办〔2019〕65号)有关精神,持续深化“放管服”改革,优化营商环境,进一步规范我省第二类创新医疗器械申报资料编写要求,指导我省企业做好第二类创新医疗器械产品申报工作,省药监局制定了《河南省第二类创新医疗器械申报资料编写指南(试行)》,现予发布。
查看详情
目的:本文通过对CRO企业客户满意度的影响因素进行筛选及重要性的排序,找出关键要素,以期为CRO企业提高客户满意度提供相关指导性建议。方法:通过文献研究法,在顾客满意理论的指导下,对CRO企业客户满意度的影响因素进行初步提取。并通过问卷调查法以及层次分析法,对提取后的因素进行筛选及重要性的排序。结果:服务质量和企业形象对CRO企业客户满意度的影响较大,服务价格的影响相对较小。结论:影响因素的重要性排序结果可作为CRO企业在服务过程中提高客户满意度的参考与依据。
查看详情
吉林为适应新冠肺炎疫情防控常态化要求,严格依法规范疫情防控医疗器械注册审评审批,指导企业合规有序开展应急审批产品延续注册工作,按照国家药监局《关于做好防控新冠肺炎疫情用医疗器械应急审批后续工作的通知》(药监综械注〔2020〕73号)要求,现就有关事项通知如下......
查看详情
为指导临床试验用医疗器械的规范管理,保证临床试验用医疗器械的安全、有效,根据《医疗器械监督管理条例》(中华人民共和国国务院令第680号)《医疗器械临床试验质量管理规范》(国家食品药品监督管理总局 中华人民共和国国家卫生和计划生育委员会令第25号)等法规文件,我局组织制定了《北京市临床试验用医疗器械管理指南》,现予以印发。
查看详情