24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

整合我国2016~2019年境内和进口的医疗器械、耗材、试剂等数据,就申报和审批情况进行解析。
查看详情
各相关单位: 为规范医疗器械注册人委托生产质量管理,明确不同主体间的质量管理责任划分,指导医疗器械注册人、受托生产企业和检查人员开展质量体系管理和核查,根据《陕西省医疗器械注册人制度试点工作实施方案》和《医疗器械生产质量管理规范》《医疗器械注册质量管理体系核查指南》,我局组织制定了《陕西省医疗器械注册人委托生产质量管理体系实施指南(试行)》,现予发布。
查看详情
2019年8月1日,国家药品监督管理局发布了《关于扩大医疗器械注册人制度试点工作的通知》(国药监械注〔2019〕33号),明确了医疗器械注册人制度由原来的3个试点省份扩大到包括湖南省在内的21个省份,现就我省开展医疗器械注册人制度试点工作政策解读如下:
查看详情
为保障医疗器械注册人制度试点工作顺利开展,根据国家药品监督管理局《关于扩大医疗器械注册人制度试点工作的通知》(国药监械注〔2019〕33号),结合本省实际,制定《湖南省医疗器械注册人制度试点工作指南(试行)》《湖南省医疗器械注册人委托生产质量管理体系实施指南(试行)》,现印发给你们,请认真贯彻实施。
查看详情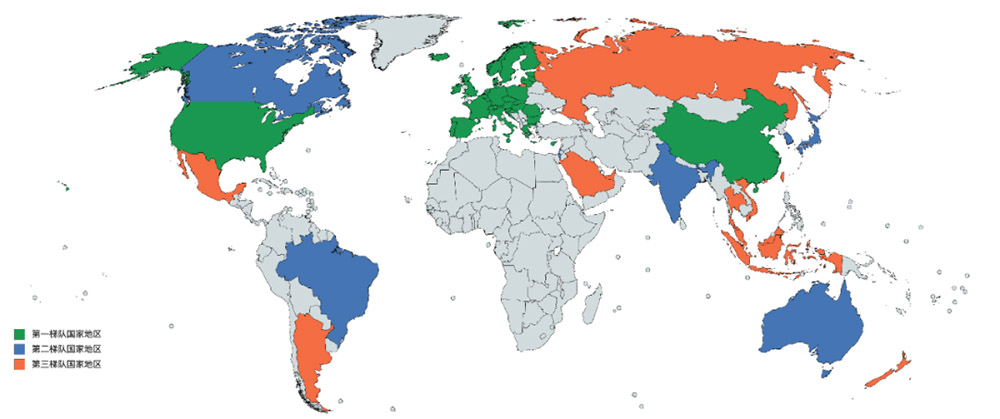
全球大部分国家地区,对医疗器械产品上市有“市场准入”的要求。各地的监管当局,主要针对医疗器械的安全性和有效性进行监管,一般分为上市前和上市后两个部分。相应地,企业被要求进行产品上市合规管控。在不同的国家和地区,大体要求基本一致,具体要求却有细枝末节的不同。无论是之前的GHTF(全球医疗器械协调工作组)还是现在的IMDRF(国际医疗器械监管者论坛),这两个协调组织,虽然都致力于建立统一的监管要求,但是,至今没有形成主要经济体之间的上市批准完全互认。
查看详情
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药品监督管理局组织制定了《无源医疗器械产品原材料变化评价指南》,现予发布。
查看详情
为切实落实“四个最严”的要求,从源头上保障医疗器械产品安全有效,江西省药品监督管理局决定对已申报的防疫用第二类医疗器械注册待审产品开展注册资料真实性专项核查。现将有关事宜公告如下。
查看详情
近日,国家药品监督管理局经审查,批准了诺沃库勒有限公司生产的创新产品“肿瘤电场治疗仪”的注册。该产品由电场发生器、电场贴片、电源适配器、电池、电池充电器、连接电缆接线盒和选配件等组成。适用于22岁及以上经组织病理学或影像学诊断的复发性幕上胶质母细胞瘤及新诊断的幕上胶质母细胞瘤。该产品为首个利用电场抑制细胞分裂原理的医疗器械,通过交变电场抑制肿瘤细胞有丝分裂过程,从而实现对胶质母细胞瘤的抑制效果。目前尚未有同类产品在国内批准上市。
查看详情