24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

本指导原则旨在指导注册申请人对下腔静脉滤器开展临床评价的资料准备,同时也为技术审评部门审评下腔静脉滤器临床评价资料提供参考。 本指导原则是对下腔静脉滤器临床
查看详情
本指导原则旨在为注册申请人在使用患者模型试验对产品进行性能研究并用于产品注册申报时提供参考,同时也为技术审评部门审评腹腔内窥镜手术系统(也称手术系统)申报资料提
查看详情
本指导原则旨在指导注册申请人对泌尿系统激光治疗设备注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对泌尿系统激光治疗设
查看详情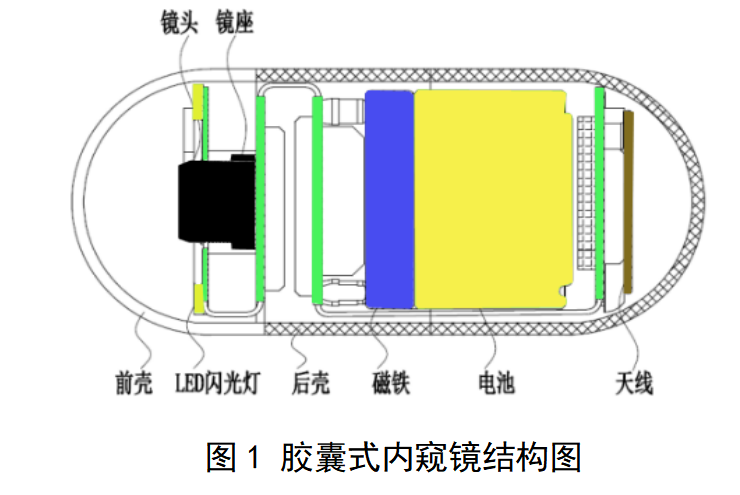
本指导原则旨在指导注册申请人对胶囊式内窥镜设备注册申报资料的准备及撰写,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对胶囊式内窥镜设备的一般
查看详情
各有关单位: 根据国家药品监督管理局医疗器械注册审查指导原则制修订计划的有关安排,我中心组织编制了《经皮冠状动脉介入生理功能检测产品注册审查指导原则(征求意见
查看详情
本指导原则旨在指导注册申请人对气管插管产品注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对气管插管产品的一般要求,申请人应依据产品的具
查看详情
本审评要点旨在指导和规范注册申请人对一次性使用球囊子宫支架类产品注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供技术参考。 本审评要点
查看详情
本指导原则旨在指导申请人对颅内取栓支架注册申报资料的准备及撰写,同时也为技术审评部门对颅内取栓支架注册申报资料的技术审评提供参考。 本指导原则系对颅内取栓支
查看详情