24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
在医疗设备维护以及需要对成本进行管控的实践情形当中,医疗机构或者是第三方服务商往往会碰到这样一个摆在眼前的现实状况,那就是当原厂CT球管呈现出价格十分高昂的态势,又或者其供应周期处于比较长的情况下,是否能够去采购其他厂家所生产制造的兼容球管来实施替换操作呢,而这一情况不单单是一个涉及技术是否能够相互匹配的问题,更是一个关乎医疗器械法规是否合规的严肃问题,就像近期贵州黔博康咨询有限公司有这样一个行为,其针对采购北京智束公司生产的CT球管可否用于上海西门子特定型号的CT设备这一事宜,向北京市药品监督管理局发出了正式的函询,从这一案例当中能够清楚地看到,解决此类问题存在着唯一的权威路径,即要深入去查询目标球管的医疗器械注册申报相关资料,尤其是其法定文件《使用说明书》。
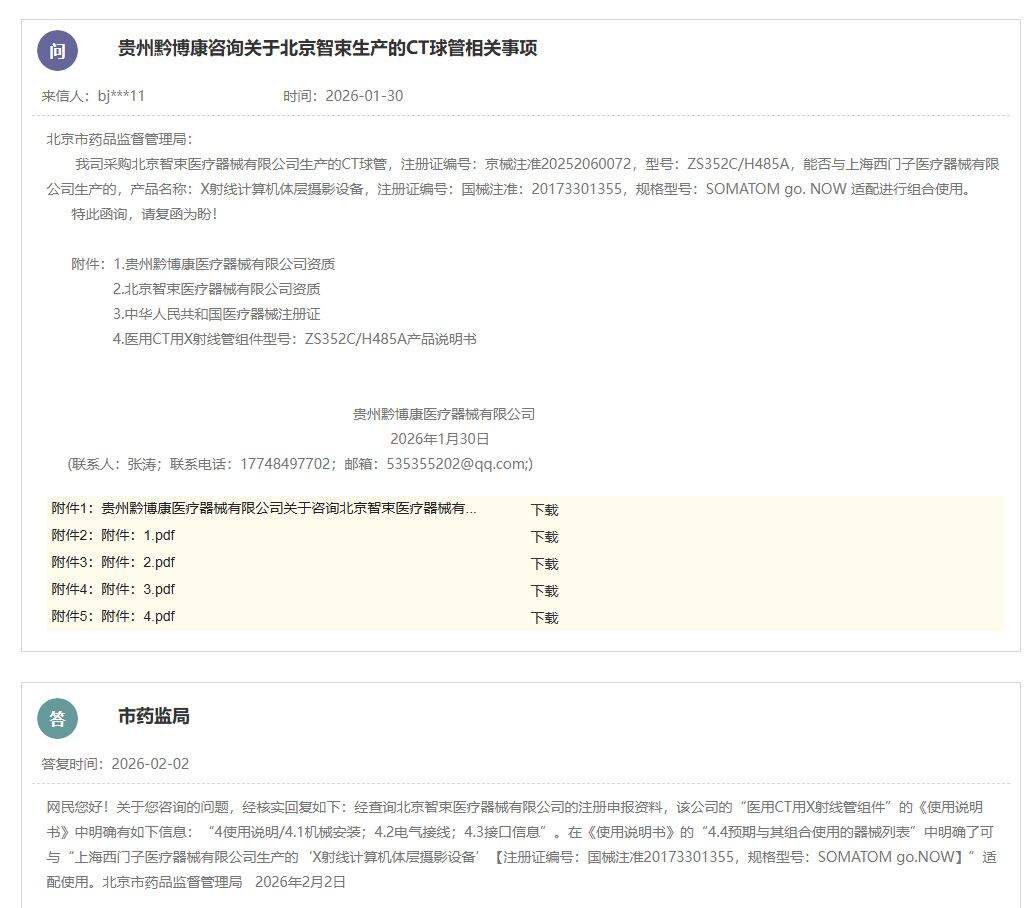
法规基石:组合使用信息必须明确载于注册资料
我国基于《医疗器械注册与备案管理办法》及相关技术审查指导原则而实行的对医疗器械的严格注册管理制度,要求当一个医疗器械的预期用途需与其他医疗器械联合使用方可实现时,申请人须于注册申报资料里详细说明,这其中不仅要明确列出预期与之组合使用的器械的生产商名称、产品具体名称、注册证编号以及规格型号等信息,还要提供相应的兼容性研究资料、风险分析资料以及验证资料,而这些经由药品监督管理部门进行技术审评并通过的内容,最终会被凝练在产品的《使用说明书》当中,使其成为具备法律效力的技术文件,所以在判断一个CT球管能否与某台CT主机相适配时,首要的且核心的依据便是该球管产品经批准的说明书里是否明确列明了该主机的相关信息。
案例解析:从官方复函看适配性确认流程
对于贵州黔博康所提具体咨询而言北京市药品监督管理局所采用的核查方式连同得出的结论具备典型示范意义,监管部门并非将判断基于单纯经验或者口头询问之上,而是选取了最为权威的核查途径,也就是把北京智束医疗器械有限公司所提交的有着注册证编号京械注准20252060072的“医用CT用X射线管组件”全套注册申报资料直接进行调取并查询,在对该产品的《使用说明书》里“4.4 预期与其组合使用的器械列表”这一关键章节加以查看时发现其中明确记载着可和上海西门子医疗器械有限公司生产的拥有注册证编号国械注准20173301355、规格型号为SOMATOM go.NOW的“X射线计算机体层摄影设备”适配使用,并且这一记载并非是简单的建议或者宣传内容,而是在注册之时所提交的电气接口匹配情况、机械结构兼容程度、控制协议一致状态以及安全有效性验证等一系列严谨研究的基础上得出的结论,同时还是经过官方审评认可的法定适配声明。
核心文件:说明书中的“预期组合使用器械列表”
对于需了解产品说明书结构与效力的医疗器械用户、采购方及技术服务商来说一份完整的医用CT球管组件说明书不但涵盖产品型号、技术参数、性能指标且会设专门章节阐述使用边界而其中作为解决跨厂家适配疑问钥匙的“预期与其组合使用的器械列表”以清单形式逐一列明经制造商验证申报并获监管机构批准的可兼容主机设备信息因目标CT主机设备的生产企业、产品名称、注册证号、型号等完整信息若清晰无误出现在该列表中则表明该组合使用的安全性和有效性在注册阶段已确认适配使用合规反之若列表未包含该主机则该组合未经官方审评认可擅自使用会面临巨大临床风险与合规风险。
实践指引:如何获取与核验关键信息
在实际操作场景当中考虑采用非原厂球管之时采购方需以主动姿态向球管供应商提出索取文件的请求并对所获文件实施严格核验流程,首当其冲的是需获取处于有效状态的《医疗器械注册证》并以此为依据对产品注册状态的合法性与有效性展开确认工作,而在这一过程中尤为关键的一点在于须获取该注册证附件部分所载明的正式《使用说明书》全文内容,采购方有必要亲自对说明书进行查阅操作并在其中定位至标题为“预期与其组合使用的器械列表”或者具备类似含义的章节板块,以逐项比对的方式就拟计划搭配使用的CT主机相关信息是否被清晰明确地列入其中这一事项开展核对工作,值得注意的是任何源自销售人员的口头承诺表述、宣传彩页当中的模糊性描述内容抑或是网页平台上所发布的兼容性声明信息,均无法对这份具备法定效力的说明书所拥有的法律效力形成替代作用,唯有通过书面形式明确记载于经相关部门批准的说明书之内的信息内容,方可被视作为合规开展使用操作的具有坚实基础的保障依据。
关于判定医用CT球管是否能够与其他厂家所生产的CT设备进行适配使用这一问题,从整体流程而言是一个具备明确法律依据以及可查证据支撑的过程,该结论的得出并非依靠主观经验判断或商业宣传内容,而完全是以球管产品注册资料当中的法定记载内容作为依据,在此过程中,医疗机构及服务商于做出采购决策之前所应履行的尽职调查义务,以及对产品说明书里所载明的“预期组合使用器械列表”进行严格核验的行为,是保障设备运行安全、影像质量稳定以及整个操作完全符合医疗器械监管法规要求的根本所在,而当出现该列表未涵盖相关设备信息或信息表述不明确的情况时,较为审慎的做法是参照贵州黔博康相关案例,向对应的药品监督管理部门提出正式的技术咨询请求以获取专业意见。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。