24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
引言:每一位参加医疗器械临床试验的受试者在正式加入受试者大家庭之前,都需要签署一份知情同意书(ICF),其中列明了受试该试验可能出现的不良情况,受试者有权不签署该协议,但不签署意味着不认可该项目,这是很矛盾的过程。
知情同意书的内容都有哪些?通过知情同意书,受试者能了解到权利义务划分、风险收益、保密情况、知情过程,以下内容将围绕这四点展开,如果你是初次作为受试者或CRC,那么如下内容你更应该了解。

一份知情同意书内,需要包含什么内容?
1、与试验相关的内容有
(1)临床试验概况;
(2)试验目的;
(3)临床试验所涉及试验性的内容;
(4)受试者参加试验的预期持续时间;
(5)参加试验的预计受试者人数;
(6)试验治疗和随机分配至各组的可能性;
(7)受试者需要遵守的试验步骤,包括创伤性医疗操作;
(8)受试者可能被终止试验的情况以及理由。
2、列明受试者的权利义务
(1)受试者的义务;
(2)受试者参加试验是自愿的,可以拒绝参加或者有权在试验任何阶段随时退出试验而不会遭到歧视或者报复,其医疗待遇与权益不会受到影响;
(3)当存在有关试验信息和受试者权益的问题,以及发生试验相关损害时,受试者可联系的研究者和伦理委员会及其联系方式;
(4)有新的可能影响受试者继续参加试验的信息时,将及时告知受试者或者其监护人。
3、受试者参加临床试验的风险收益
(1)临床预期的获益,以及不能获益的可能性;
(2)试验可能导致受试者的风险或者不便,尤其是存在影响胚胎、胎儿或者哺乳婴儿的风险时;
(3)其他可选的药物和治疗方法,及其重要的潜在获益和风险;
(4)受试者发生与试验相关的损害时,可获得补偿以及治疗;
(5)受试者参加临床试验可能获得的补偿;
(6)受试者参加临床试验预期的花费。
4、保密情况
(1)在不违反保密原则和相关法规的情况下,监查员、稽查员、伦理委员会和药品监管部门检查人员可能查阅受试者的原始医学记录,已核实临床试验的过程和数据。
(2)受试者相关身份鉴别记录的保密事宜,不公开使用,如果发布临床试验结果,受试者的身份信息仍保密。
5、知情过程及要点
(1)知情同意书审核:伦理委员会审核,申办方获得书面审查意见(同意)。
(2)项目启动会培训:研究者得到培训,获得授权。
(3)合适受试者:受试者相关检查符合方案固定(包含检查时间)。
(4)知情同意:研究者实施知情过程;受试者本人/受试者监护人、公正见证人(若适用)、研究者签署姓名、知情时间病程记录知情的过程,知情的具体时间。
(5)文件保存:受试者获得一份知情同意书
(6)后续跟进:是否有新版知情同意书。
谁来签署知情同意书?
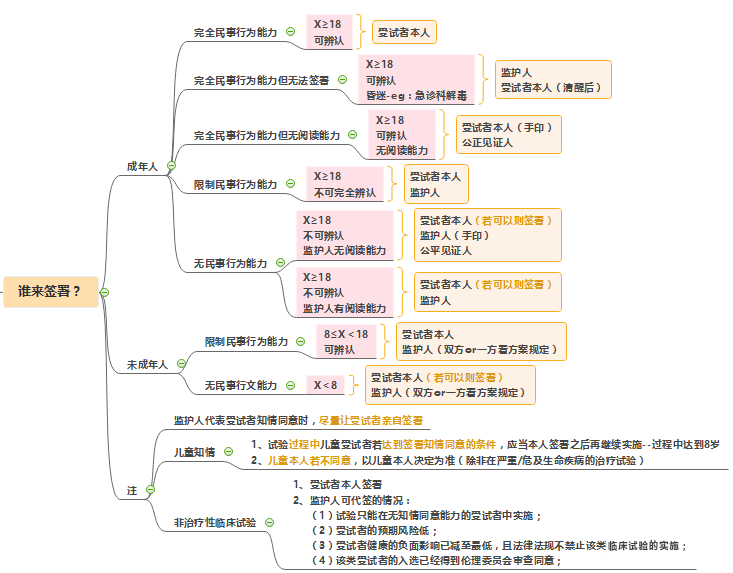

CRA需要关注哪些?(可能不全,待补充)
1、版本日期:EC通过的最新版;
2、页码:页码是否完整?是否有无缺页、是否有字迹不清晰的情况?
3、签署人:
(1)受试者:a. 几周岁?—监护人的任务关系是否说明? b. 是否具有阅读能力?—公正见证人的人物关系是否说明? c. 是否有辨认识别能力?—监护人的人物关系是否说明? d. 儿童受试者试验过程中是否达到8岁?
(2)其他相关人员:是否具有阅读能力?
(3)研究者:是都被授权、被培训?
(4)字迹是否可辨认。
4、签署时间:时间是否具体?是否是签署知情后开始试验筛选流程?
5、病程记录:是否记录知情过程,包含具体知情时间?
6、统一:ICF、CRF、SD、病程记录......是否统一?
7、文件保存:受试者是否带走一份?

可能出现的问题有哪些?(待补充)
1、知情签署的版本号有误:
(1)立马解决—重新进行知情,签署经过EC批准的最新版知情;
(2)事件人—对相关责任人员进行培训;
(3)事件物—对未用/不适用的文件进行封存,保留相应的记录。
2、入组过程中,知情版本更新:
(1)立马解决:已经入组的重新签署,下次随访期较近的安排签署计划,下次随访期较远的先电话沟通联系,保证未出组受试者人手两份知情,一新一旧;新入组的签署新版知情,注意检查版本日期,避免混淆。
(2)事件人:伦理备案;受试者重新知情;研究者重新培训;
(3)事件物:过程文件记录。
来源:Mou-小正医学
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
下一篇:CRA监查内容及现场监查注意要点