24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
GCP的培训主要是线上和线下,线上的培训安排时间较长,可为几周或几个月;线下的培训通常为一周时间,两者考完即发放GCP证书。先了解一下现在的GCP报名渠道吧!
查看详情
怎么取得GCP证书?北京有GCP培训的地方吗?北京市GCP证书线上培训班来啦!飞速度开展GCP培训,具备GCP证书发放资质,效力等同高研院,支持备案。GCP证书是进入临床行业的敲门砖,在CRO公司、医疗机构及各大生产企业应用广泛。目前飞速度已为超过400名有需求的小伙伴,成功发放GCP证书。

截止2021年6月7日,已有2124家医院成为药物/医疗器械GCP备案机构,越来越多的医生、医院承担起了临床试验的职责。尽管前期投入多,医生很辛苦,但是会“苦尽甘来”的,这可能是许多医院对GCP的理解。但临床项目带来的丰厚利润,也让备案机构有更好的发展,来提高服务质量和购买更加优质的医疗设备。
查看详情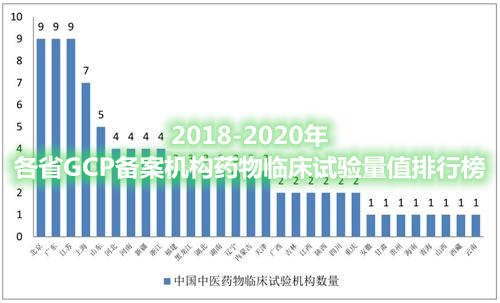
2021年1月3日,在中国药学会药物临床评价研究专委会的指导下,CCHRPP携手药研社发布了《CCHRPP全国GCP机构药物临床试验量值》榜单,以各类药物临床试验数量为基本数据,统计八项客观指标加权量值,经加和获得总分排名,展现了全国前200家药物临床试验机构对医药研发领域贡献度和影响力。现将各省/直辖市2018-2020年试验量值综合分20分以上的GCP机构以图表形式列出,同步形成各省GCP机构综合排行榜,供各界人士参考。
查看详情
GMP、GLP和GCP是什么?GMP(GOOD MANUFACTURING PRACTICE)良好生产规范:世界卫生组织将GMP定义为指导食物、药品、医疗产品生产和质量管理的法规。GMP要求制药、食品等生产企业应具备良好的生产设备,合理的生产过程,完善的质量管理和严格的检测系统,确保产品质量(包括食品安全卫生)符合法规要求。对此标准的监督与实施是由FDA来执行。
查看详情
本文主要围绕目前市面GCP证书认可度最高的培训机构——国家药监局高研院gcp考试时间展开,说明一下考试周期和逾期处理。
查看详情
GCP及临床试验流程ppt免费下载啦!文章底部自行下载!
查看详情
江西省二类医疗器械注册怎么注册?我们在此特地列出来供大家参考了解: 受理条件 【予以批准的条件】 申请资料符合要求,且通过了医疗器械注册质量管理体系核查,符合安
查看详情