24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

良好生产规范:世界卫生组织将GMP定义为指导食物、药品、医疗产品生产和质量管理的法规。GMP要求制药、食品等生产企业应具备良好的生产设备,合理的生产过程,完善的质量管理和严格的检测系统,确保产品质量(包括食品安全卫生)符合法规要求。对此标准的监督与实施是由FDA来执行。
药物非临床研究质量管理规范:药物的非临床研究是指非人体研究,亦称为临床前研究,用于评价药物的安全性,在实验室条件下,通过动物实验进行非临床(非人体)的各种毒性实验,包括单次给药的毒性试验、反复给药的毒性试验、生殖毒性试验、致突变试验、致癌试验、各种刺激性试验、依赖性试验以及与药品安全性的评价有关的其他毒性试验。我国的《药品非临床研究质量管理规范》于1999年发布并于1999年11月1日起施行。对此标准的监督与实施是由FDA来执行。
药品临床试验管理规范:规范药品临床试验全过程的标准规定,其目的在于保证临床试验过程的规范,结果科学可靠,保护受试者的权益并保障其安全。GCP不但适用于承担各期(I--IV期)临床试验的人员(包括医院管理人员、伦理委员会成员、各研究领域专家、教授、医师、药师、人员及实验室技术人员),同时也适用于药品监督管理人员、制药企业临床研究员及相关人员。对此标准的监督与实施是由FDA来执行。
USP是产品与检测方法的标准。FDA对药品和营养补充剂的管理引用部分USP标准。但不是所有USP标准都是被法律化的。FDA负责监督和实施GxP的执行。
制药业重要规范统称药品GxP,包括常见的GMP、GLP和GCP-以下分析三者区别:
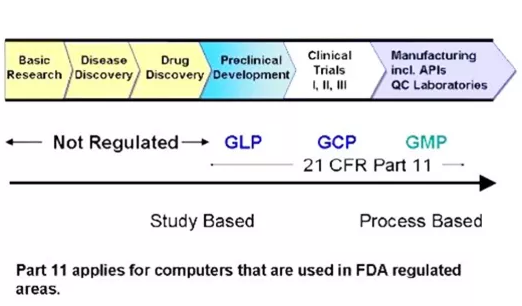
在GMP、GLP和GCP的规范下,药品的质量可控性、安全性和有效性由各项试验得到充分证据,注册申报通过审查,药品被批准上市。目的达到,交集完成了使命。非临床研究不再,GLP就结束了;如果有上市后临床试验,GCP必不可少;只要产品不撤市,生产继续,GMP就无止境。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。