24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

医疗器械从研发到上市,必须通过临床试验验证其安全性和有效性。对于医疗机构来说,想要参与这类试验,必须先完成“临床试验机构备案”。截至2024年6月,全国已有138
查看详情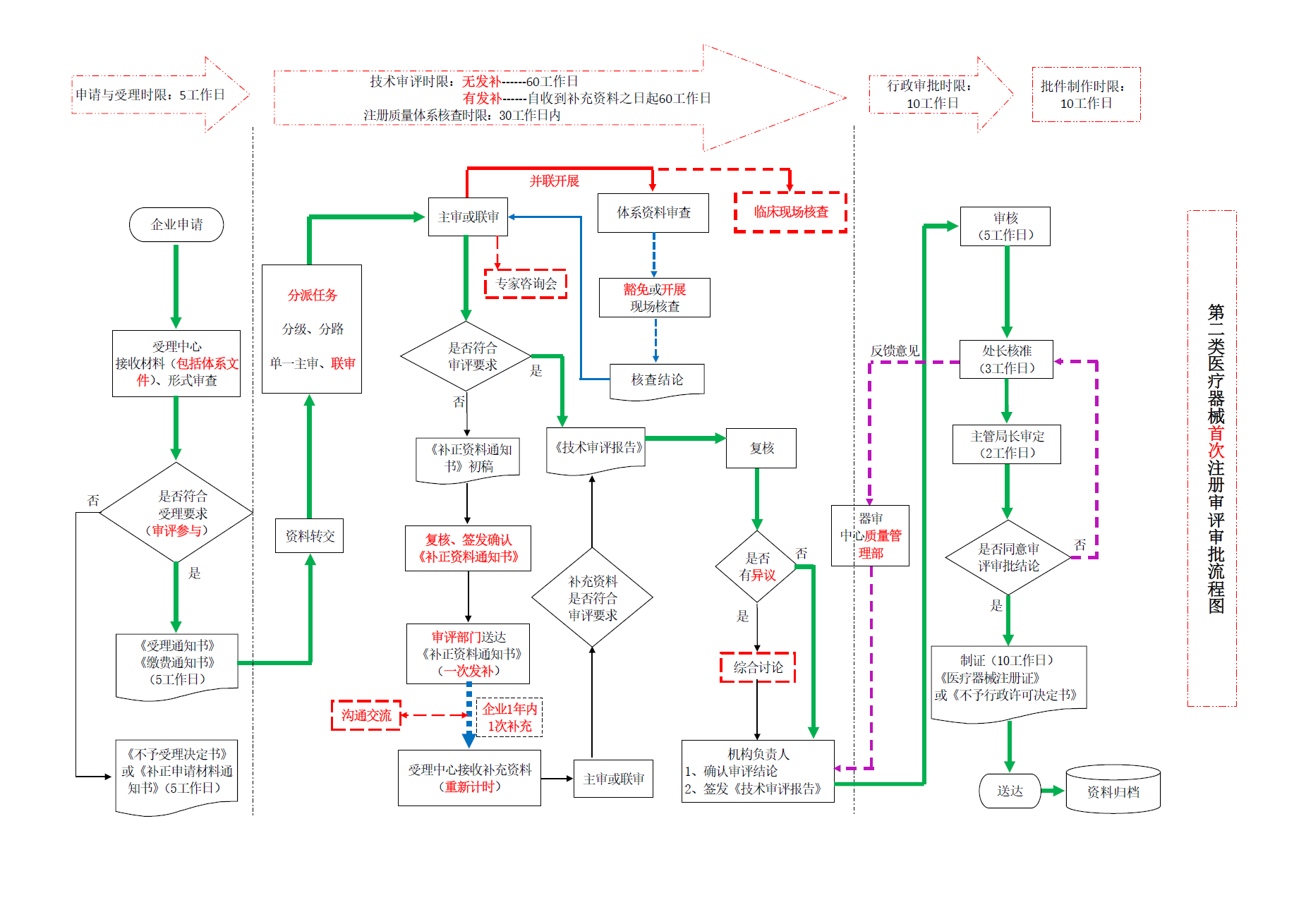
医疗器械作为医疗领域的重要工具,其安全性和有效性直接关系到患者的健康。在我国,医疗器械按照风险等级分为三类,第二类医疗器械需要经过严格的注册审批才能上市销售。上海
查看详情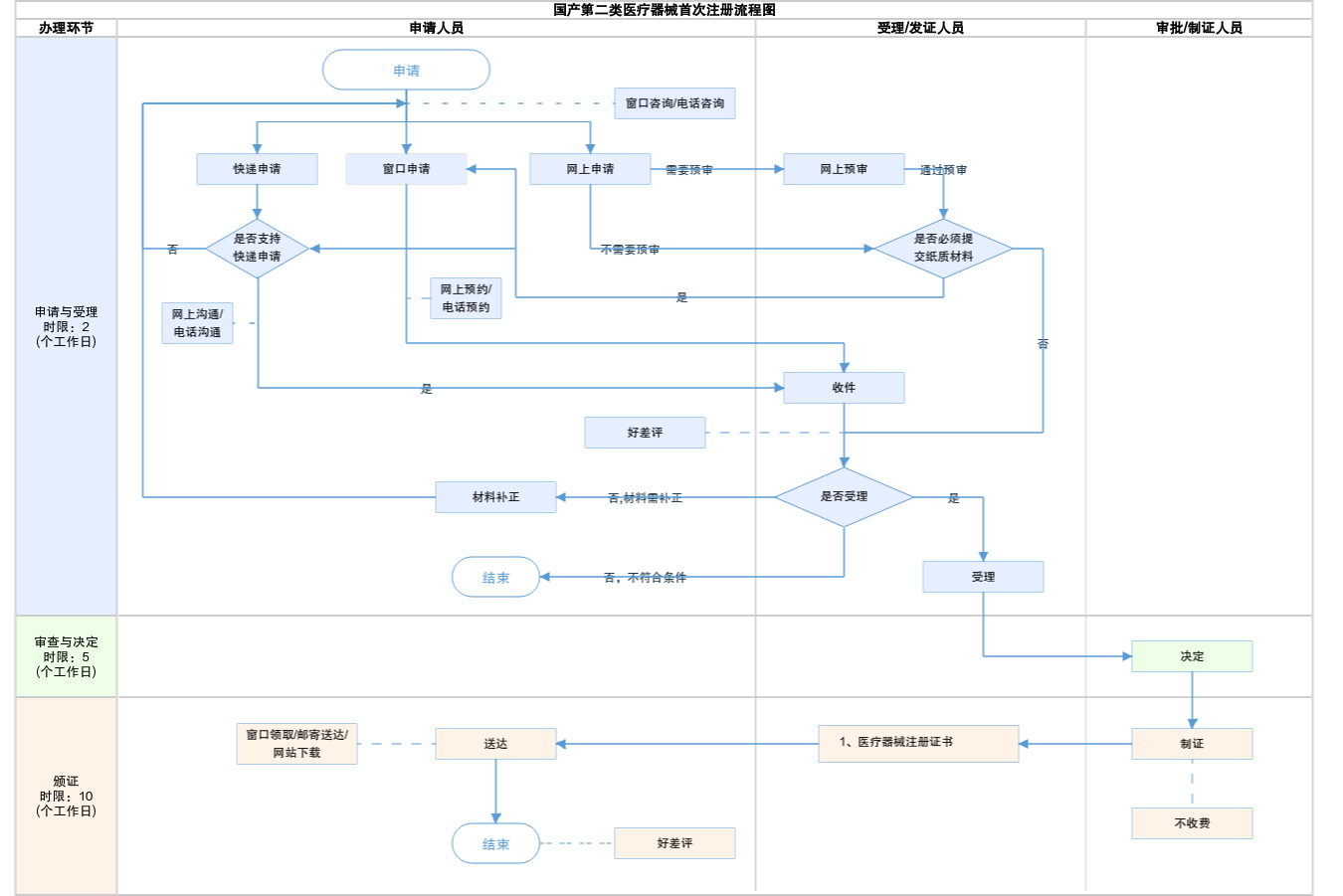
想要把自家的医疗器械产品推向市场,注册手续是绕不开的环节。很多企业觉得这事儿复杂得像走迷宫,特别是对血压计、血糖仪这类风险中等的第二类医疗器械,到底需要准备哪些材
查看详情
2025年4月,河南省药品监督管理局共批准注册第二类医疗器械产品101个,具体产品详见附件。 特此公告。 附件:2025年4月批准注册医疗器械产品目录 2025年5月9日2025
查看详情
牙齿龋坏或缺损时,填充材料与器械的协同作用决定了修复效果。围绕《口腔硬组织用填充材料的器械及操作原理描述需考虑哪些内容》,本文将用通俗语言拆解核心要点,帮助理解这
查看详情
在体外诊断领域,核酸扩增法检测试剂的应用越来越广泛。这类试剂的核心是核酸扩增反应液,它直接决定了检测的灵敏度和准确性。但很多企业在申报注册时,面对商用反应液的多组
查看详情
我国手术机器人从“技术跟随”迈向“全球首创”,迎来新突破。近日,国家药监局批准了上海微创医疗机器人(集团)股份有限公司(以下简称微创机器人公司)
查看详情
日前,由河北省药物警戒中心牵头、承德市药品不良反应监测中心、河北医科大学第三医院等单位共同起草的地方标准《医疗机构药物警戒技术规范》(编号DB13/T 6072-2025)正式
查看详情