24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
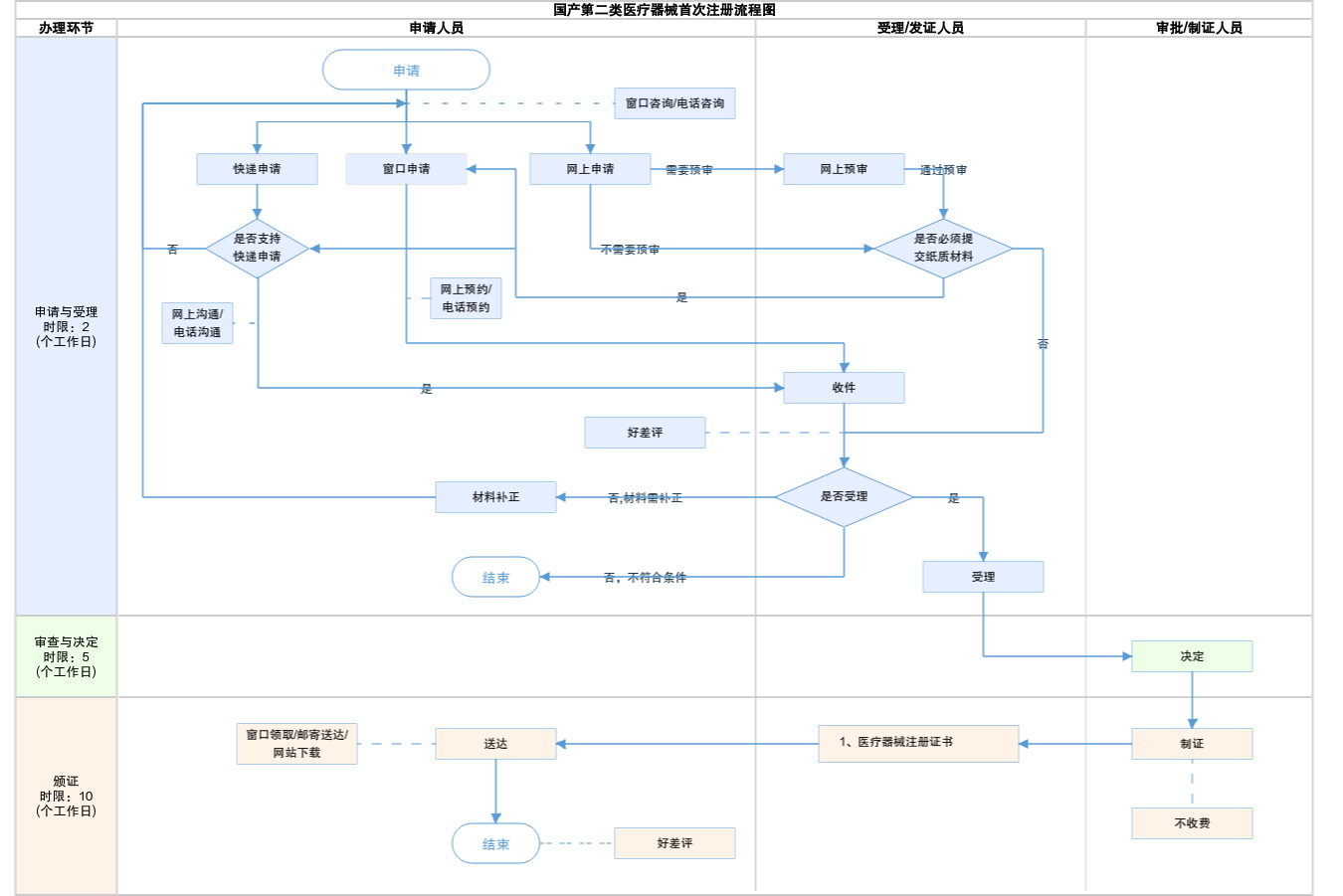
想要把自家的医疗器械产品推向市场,注册手续是绕不开的环节。很多企业觉得这事儿复杂得像走迷宫,特别是对血压计、血糖仪这类风险中等的第二类医疗器械,到底需要准备哪些材料?审核要多长时间?今天咱们就拆解北京市的具体流程,用大白话讲清楚每一步该做什么。
第一步 材料备齐再出手
注册这事儿最怕缺材料被打回来。北京市药监局官网上明确列了八项必备材料,咱们可以分成三个大类来准备:
| 材料类型 | 具体内容 |
|---|---|
| 基础信息类 | 产品注册申请表(选体外诊断试剂或普通器械版本)、授权委托书(委托代办时需要) |
| 技术证明类 | 产品说明书和标签样稿、质量管理体系文件(生产车间的质量管控记录) |
| 安全验证类 | 临床评价资料(检测报告或临床试验数据)、非临床资料(比如实验室性能测试) |
去年有家企业交材料时漏了生产环境检测报告,结果整个流程卡了两个月。建议先把所有文件扫描成PDF,用文件夹分类命名,比如“01申请表”“02说明书”。
第二步 选对路子交申请
北京市现在提供三种申请方式,就跟点外卖选配送方式似的:
1.网上快速通道(适合老手)
登录北京市政务服务网传材料
系统自动预审,2小时内出受理结果
适合之前注册过同类产品的企业
2.窗口现场办理(适合需要指导的)
提前电话预约(别直接冲过去容易扑空)
带着纸质材料到丰台区政务服务中心
工作人员当面核对,缺啥马上补
3.邮寄申报(疫情期间很多人选这个)
顺丰寄到指定地址(记得备注联系人电话)
收到后会有短信通知
最近有企业尝试网上申请,结果把产品说明书传成了旧版本,被系统自动退回。建议上传前让两个同事交叉检查文件名和内容。
第三步 盯紧进度别松懈
材料交上去之后,官方给出的时间线是这样的:
1.受理阶段(2个工作日)
工作人员检查材料齐不齐
收到短信通知受理结果
如果让补材料,20天内要重新交齐
2.审核阶段(5个工作日)
专家组看技术资料是否达标
可能会接到核查电话(保持联系人手机畅通)
这个阶段最容易出问题,比如某企业的血糖仪临床数据样本量不足
3.发证阶段(10个工作日)
制证完成后可选窗口自取或快递到家
电子证书同步发到企业账号
记得检查证书上的产品名称和型号对不对
上个月有家企业拿到证后才发现生产地址写错了一个字,又得重新申请变更。建议领证时带公章当场核对。
第四步 后续事项要门儿清
拿到注册证可不是万事大吉了,这些事得记在小本本上:
1.生产许可衔接:注册证到手后30天内要办生产许可证
2.定期提交报告:每年3月底前交上年度质量管理自查报告
3.变更早知道:如果换原材料供应商或改生产工艺,记得提前备案
有家生产医用口罩的企业,去年因为换了熔喷布供应商没备案,被抽查时罚了五万块。涉及产品核心部件的变动千万别自己悄悄改。
避坑指南
根据北京市药监局2023年的数据,注册被退回的三大原因分别是:
1.临床评价资料不全(占42%)
2.生产体系文件造假(占35%)
3.产品技术要求不达标(占23%)
特别是体外诊断试剂类产品,很多企业栽在参考区间验证上。比如某企业的幽门螺杆菌检测试剂,参考值范围直接照搬国外数据,没考虑中国人饮食习惯差异,结果审评没通过。
政策红利别错过
北京市从2022年开始推行二类医疗器械注册全程网办,还搞了几个贴心服务:
1.预审辅导:提交前可预约专家在线预审材料
2.加急通道:对抗疫类产品开放绿色通道(最快15天拿证)
3.零跑动套餐:从申请到领证全程线上完成
之前有个做康复器械的创业公司,通过预审服务提前修改了六处材料问题,一次性通过审核。这种羊毛该薅就得薅,建议找飞速度CRO这样的专业的第三方CRO公司来处理,一次过早点创造效益,并实施掌握政策动态
整个流程走下来,顺利的话大概两个月能搞定。关键是把材料准备扎实,别想着走捷径。现在政府办事透明度高,官网随时能查进度,遇到问题打12345转药监专线也挺管用。记住医疗器械注册不是搞突击战,而是持久战,前期准备越充分,后面越省心。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。