24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

截止21年2月2日,药监总局对于目前指定已备案医疗器械临床试验机构清单进行了变更,据临床试验机构清单介绍,目前已备案机构已达998家,覆盖30个省区直辖市。下列表格中的临床试验机构清单是2021年药监总局认可的可开展医疗器械临床试验的已备案机构,文末提供word下载哦。
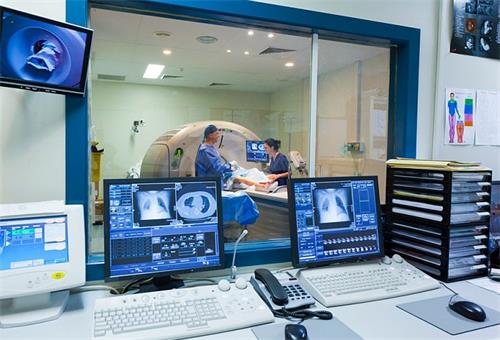
国家药监局关于发布医用磁共振成像系统同品种临床评价技术审查指导原则(2020年修订版)的通告(2021年第12号)发布时间:2021-02-01为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药监局组织制定了医用磁共振成像系统同品种临床评价技术审查指导原则(2020年修订版)(见附件),现予发布。特此通告。
查看详情
医用磁共振成像系统同品种临床评价技术审查指导原则(2020年修订版)为进一步规范医用磁共振成像系统(简称MR系统)的同品种临床评价,撰写本指导原则。本指导原则是对2017年发布《医用磁共振成像系统临床评价技术审查指导原则》的修订。本指导原则是对注册申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
查看详情
国家食品药品监督管理总局关于发布医疗器械产品技术要求编写指导原则的通告(第9号)
发布时间:2014-05-30国家食品药品监督管理总局通告2014年第9号关于发布医疗器械产品技术要求编写指导原则的通告为规范医疗器械注册管理工作,根据《医疗器械监督管理条例》(国务院令第650号),国家食品药品监督管理总局组织制定了《医疗器械产品技术要求编写指导原则》,现予发布。

影像型超声诊断设备新技术注册技术审查指导原则(2015年第33号)本指导原则是对影像型超声诊断设备中部分新型技术的一般要求,申请人/制造商应依据具体产品的特性对注册申报资料的内容进行充实和细化,并依据具体产品的特性确定其中的具体内容是否适用,若不适用,需详细阐述其理由及相应的科学依据。本指导原则是对申请人/制造商和审查人员的指导性文件,但不包括审评审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。应在遵循相关法规的前提下使......
查看详情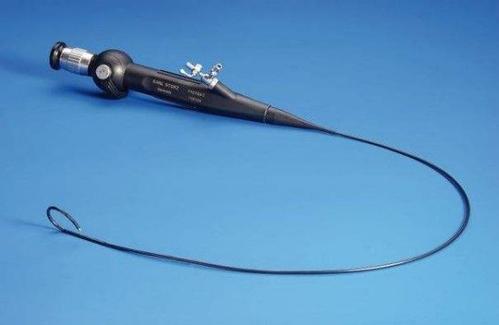
随着医疗器械分类及免临床医疗器械目录的调整,部分电子内窥镜产品的管理类别从III调整为II类,同时列入免于进行临床试验的医疗器械目录,因此在注册申报过程中,其注册申报要求和流程都将应根据最新法规进行调整应对。
查看详情
随着互联网和信息技术的飞速发展,信息技术的各项应用也越来越广泛和普及。作为生活和工作不可或缺的载体和手段,网络和信息技术在带来便利的同时,也衍生出了许多新的问题,其中网络信息安全问题直接关系到国家、组织和公民的安全和切身利益,解决这一问题迫在眉睫。
查看详情
兜兜转转,否极泰来,终于成为一名CRA。首先感谢药物临床试验网里各位朋友的分享,我在这里学习了很多知识,这在我面试过程中给了我很大的帮助。本人前天收到了一家名企(就叫它A公司吧)CRA的offer,一波三折,终于真正能踏入CRA这一行业。
查看详情