24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

随着互联网和信息技术的飞速发展,信息技术的各项应用也越来越广泛和普及。作为生活和工作不可或缺的载体和手段,网络和信息技术在带来便利的同时,也衍生出了许多新的问题,其中网络信息安全问题直接关系到国家、组织和公民的安全和切身利益,解决这一问题迫在眉睫。
查看详情
兜兜转转,否极泰来,终于成为一名CRA。首先感谢药物临床试验网里各位朋友的分享,我在这里学习了很多知识,这在我面试过程中给了我很大的帮助。本人前天收到了一家名企(就叫它A公司吧)CRA的offer,一波三折,终于真正能踏入CRA这一行业。
查看详情
临床试验如何管理生物样本?本篇我们通过一个案例简洁明了了解管子应该如何管理!!!在2020.6某项目随访完成后,中心实验室提出质疑:2号患者免疫原性分离管缺失,需要患者重新来院采集样本检测。CRC开始回想,1号、2号患者同时来院随访,随访周期一样,样本采集要求一样。既然1号无误,应该是错把2号免疫原性分离管写为1号。与中心实验室再次核实,1号患者无误。但是中心实验室不承认此项结果,需要重新采集2号患者缺失样本。
查看详情
当医疗器械必须以无菌的形式提供时(比如生产医用外科口罩等),在其灭菌前应将各种非预期的微生物污染降至最低。因此,其生产场地、生产环节等都需要进行严格的无菌要求和控制。为了保障无菌医疗器械的生产过程符合要求,在生产环境、质量控制等环节要进行必要的验证和确认。本文按照GMP的顺序,把无菌医疗器械生产需做的验证和确认项目整理如下,供大家参考。
查看详情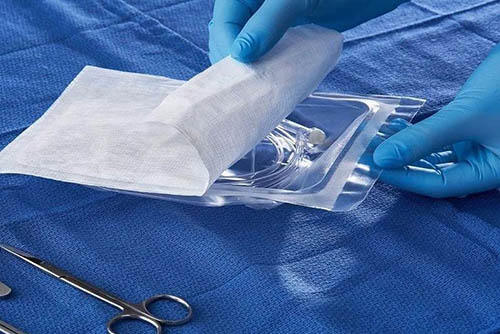
无菌医疗器械的包装使无菌医疗器械保持无菌性和完整性,因此,无菌医疗器械的包装必须可提供阻隔微生物和物理防护的功能,并可标识产品的相关信息,故而其材料的选择应结合预期内包装物的实际情况并进行全面评价。本文整理了对无菌医疗器械包装进行全面评价的几点要求,供大家参考。
查看详情
从1月1日起,列入《第一批实施医疗器械唯一标识的产品目录》的产品首次注册、延续注册或者注册变更时要填产品标识(UDI-DI)。为了让大家更好的完成产品注册工作,小编从整理了下面这份内容:
查看详情
标准号:GB/T 16886.3-2019。中文标准名称:医疗器械生物学评价 第3部分:遗传毒性、致癌性和生殖毒性试验。英文标准名称:Biological evaluation of medical devices—Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity
查看详情
为规范和统一国内对适应性设计的认识,促进适应性设计的应用和理解以提高研发效率,药审中心组织制定了《药物临床试验适应性设计指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
查看详情