24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

α-氰基丙烯酸酯类医用粘合剂注册技术审查指导原则(2016年第6号)本指导原则旨在帮助和指导申请人对α-氰基丙烯酸酯类医用粘合剂产品注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工作的质量和效率。本指导原则是对α-氰基丙烯酸酯类医用粘合剂产品注册申报资料的一般要求,申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化。申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
查看详情
一次性使用膜式氧合器注册技术审查指导原则(2016年第6号)本指导原则旨在给出一次性使用膜式氧合器(以下简称“膜式氧合器”)产品注册具有指导意义的指南性文件,一方面有利于监管部门对膜式氧合器上市前的安全性和有效性进行准确、高效的评价,另一方面有利于指导企业规范产品的研究和生产。本指导原则系对膜式氧合器的一般要求,生产企业应依据具体产品的特性对注册申报资料的内容进行充实和细化。生产企业还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需详细阐述其理由及相应的科学依据。
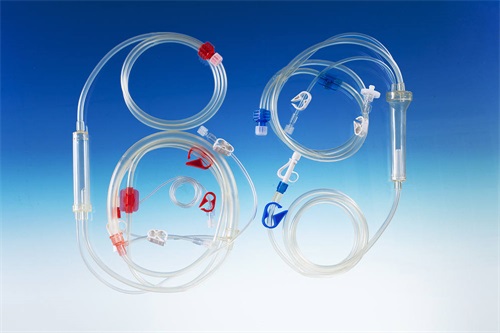
一次性使用血液透析管路注册技术审查指导原则(2016年第146号)本指导原则旨在指导注册申请人对一次性使用血液透析管路(以下简称血透管路)注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则系对血透管路的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情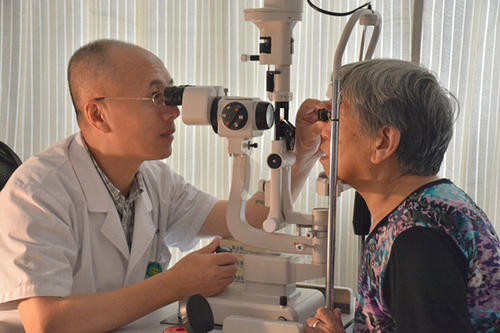
眼科超声乳化和眼前节玻璃体切除设备及附件注册技术审查指导原则(2016年第162号)本指导原则旨在给出系统的、具有指导意义的指南性文件,用于指导注册申请人规范产品的研究开发和注册申报,同时也用于指导监管部门对眼科超声乳化和眼前节玻璃体切除设备及附件申请注册材料的技术审评。本指导原则系对眼科超声乳化和眼前节玻璃体切除设备及附件的一般要求,注册申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化。注册申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需详细阐述其理由及相应的科学依据。
查看详情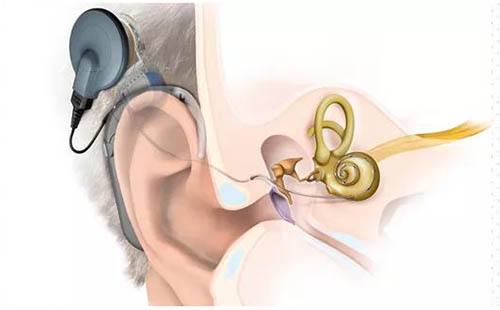
人工耳蜗植入系统临床试验指导原则(2017年第3号)目的:为进一步规范指导人工耳蜗植入系统产品的临床试验,按照《医疗器械临床试验质量管理规范》,撰写本指导原则。本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时调整。
查看详情
袜型医用压力带注册技术审查指导原则(2017年第14号)本指导原则旨在指导注册申请人对袜型医用压力带注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对袜型医用压力带的一般要求,申请人应依据具体产品特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情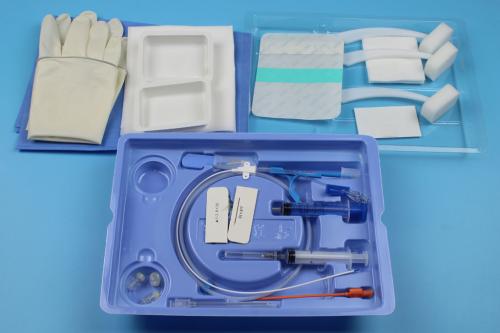
中心静脉导管产品注册技术审查指导原则(2017年第14号)本指导原则旨在帮助和指导申请人对中心静脉导管产品注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工作的质量和效率。本指导原则是对中心静脉导管产品注册申报资料的一般要求,申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化。申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
查看详情
钙磷/硅类骨填充材料注册技术审查指导原则(2017年第14号)本指导原则旨在为申请人进行钙磷/硅类骨填充材料的注册申报提供技术指导,同时也为食品药品监督管理部门对注册申报资料的审评提供技术参考。本指导原则系对钙磷/硅类骨填充材料注册申报资料的一般要求,申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化,并依据具体产品的特性确定其中的具体内容是否适用。
查看详情