24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

国家药监局关于发布家用体外诊断医疗器械注册技术审查指导原则等7项注册技术审查指导原则的通告(2020年第80号),为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药品监督管理局组织制定了《家用体外诊断医疗器械注册技术审查指导原则》《特定蛋白免疫分析仪注册技术审查指导原则》《泌乳素检测试剂注册技术审查指导原则》《总三碘甲状腺原氨酸检测试剂注册技术审查指导原则》《25-羟基维生素D检测试剂注册技术审查指导原则》《血清淀粉样蛋白A检测试剂注册技术审查指导原则》和《类风湿因子检测试剂注册技术审查指导原则》,现予发布。
查看详情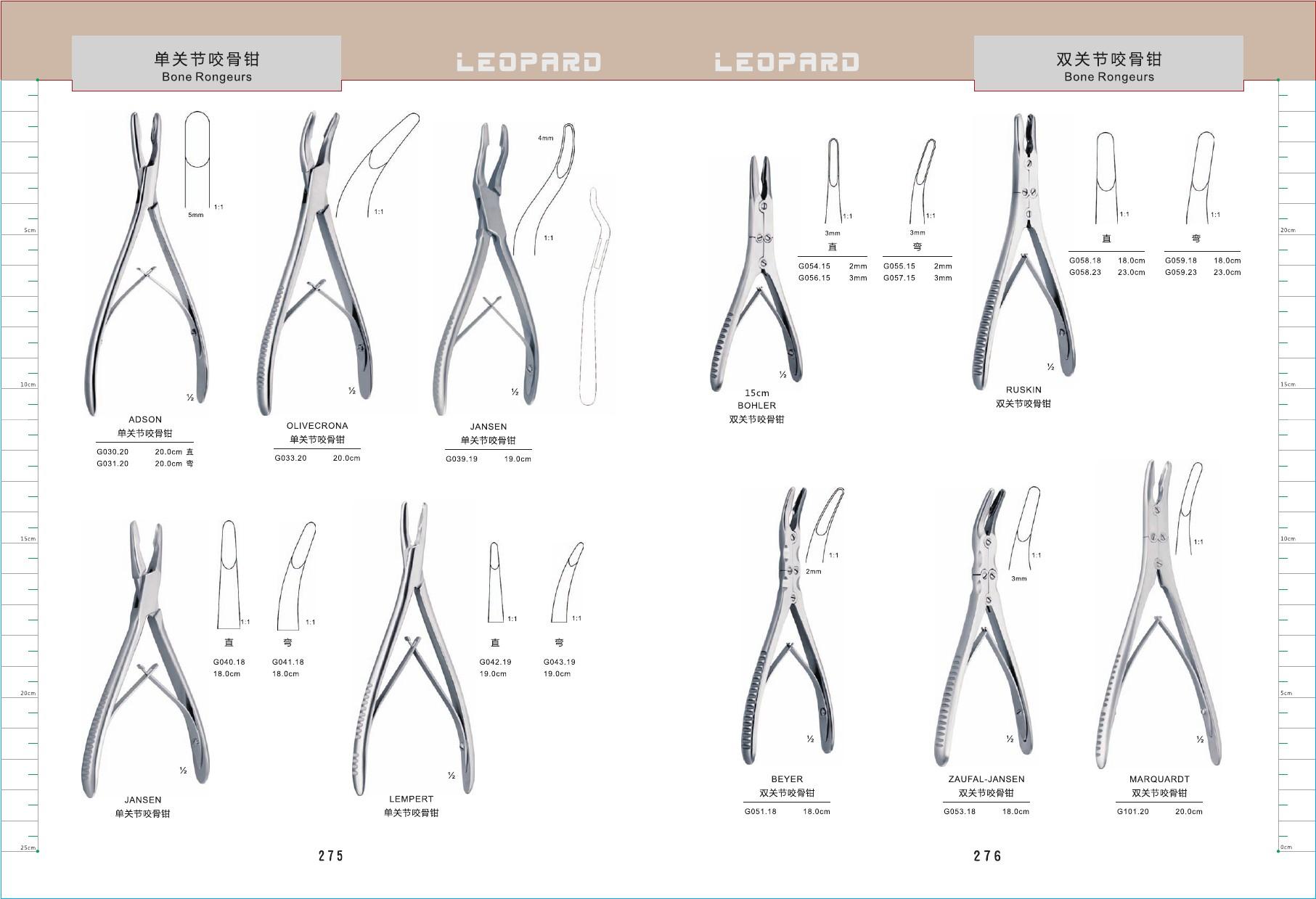
为进一步规范医疗器械通用名称,加强医疗器械全生命周期管理,国家药品监督管理局组织制定了《骨科手术器械通用名称命名指导原则》《输血、透析和体外循环器械通用名称命名指导原则》《无源手术器械通用名称命名指导原则》《无源植入器械通用名称命名指导原则》和《医疗器械消毒灭菌器械通用名称命名指导原则》,现予发布。
查看详情
对于医疗器械领域来说,创新是永远的话题。随着集采风暴压境,越来越多高值耗材进入低值时代,医械行业的创新进程也开启了加速模式。对于械企来说,要想更长远的发展,必须创新研发,从而避免同质化产品进入集采的命运。每个创新产品的出现,对行业都有里程碑式的意义。细数骨科史上,那些惊艳业内的创新产品,如关节镜、Ilizarov外固定架等,都带来了划时代的变革。那么未来骨科领域的颠覆性创新又会出现在哪些技术/产品上呢?
查看详情
12月3日,中国药品监督管理研究会、清华大学老科协医疗健康研究中心与社会科学文献出版社联合发布了《医疗器械蓝皮书:中国医疗器械行业发展报告(2020)》(以下简称《报告》)。《报告》从多角度论述了2019年影响医疗器械行业发展的政策变化态势。审批制度改革方面,提出要不断健全医疗器械标准管理体系......
查看详情
北京市药品监督管理局(以下简称市药监局)各分局定于12月1日起正式履职。依据相关法律法规,经研究,就分局职责、管辖范围和履职后市区两级药品、医疗器械和化妆品监管业务调整情况公告,内含各分局管辖范围和联系方式。......
查看详情
近日,为进一步优化营商环境,提升政务服务效能,最大限度减少企业跑腿次数、压缩办理时间、降低办事成本,河南省药监部门再次提升办事效率,服务事项的受理送达方式再次缩短,百姓办事不再难!
查看详情
北京药监各分局履职后,发布最新的医疗器械生产许可和生产备案工作公告。其中包括:医疗器械生产相关事项办理及其程序、对于《医疗器械生产许可证》有关事项、对于第一类医疗器械生产备案、对于办理委托生产备案、对于办理医疗器械出口销售证明......
查看详情
为贯彻落实《中华人民共和国药品管理法》关于建立药物警戒制度的要求,规范药品上市许可持有人药物警戒主体责任,国家药品监督管理局起草了《药物警戒质量管理规范(征求意见稿)》,现向社会公开征求意见。请于2020年12月18日前,将有关意见或建议通过电子邮件形式反馈至ypjgs@nmpa.gov.cn,邮件标题请标明“药物警戒质量管理规范意见反馈”。
查看详情