24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

2024年12月,江西省药品监督管理局共批准注册境内第二类医疗器械产品20个(具体产品见附件)。 特此公告。 附件:2024年12月批准注册医疗器械产品目录.pdf 江西省药
查看详情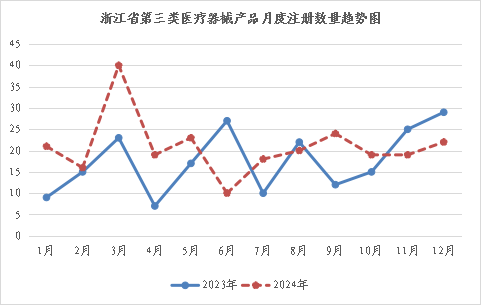
根据国家药品监督管理局2025年第4号公告,2024年12月,国家药品监督管理局共批准注册境内第三类医疗器械产品212个。 我省医疗器械生产企业获得国家局批准注册第三类医疗
查看详情
2024年12月,浙江省内各市市场监督管理局共新备案第一类医疗器械产品332个,其中有源类9个,无源类81个,体外诊断试剂242个(具体产品见附件)。 按照备案人所在辖区分析,杭州
查看详情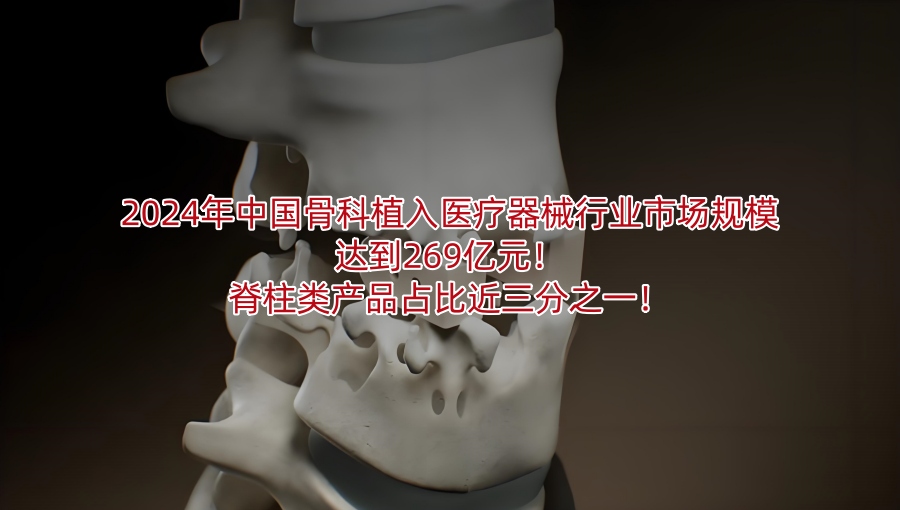
随着中国人口老龄化的加剧和医疗技术的不断进步,骨科植入医疗器械市场迎来了前所未有的发展机遇。根据最新数据统计,2024年中国骨科植入医疗器械行业的市场规模预计将达到
查看详情
序号 产品名称中文* 申请人名称* 注册号* 备注 1 透明质酸修护生物膜敷料 西安朴若医疗科技有
查看详情
2024年12月,河北省药品监督管理局共批准首次注册第二类医疗器械产品56个(详见附件)。 特此公告。 附件:2024年12月批准首次注册第二类医疗器械产品目录.pdf 河北
查看详情
根据《医疗器械监督管理条例》相关规定,现将2024年12月广西药监局审批的第二类医疗器械产品注册信息予以公布。 文件下载: 2024年12月第二类医疗器械产品注册信息.x
查看详情
2024年12月进口第一类医疗器械产品备案信息 序号 产品名称 备案号 备案人名称原文 生产地址原文 备案日期 状态 1 待测物清洗液 国械备2
查看详情