24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

药品经营质量管理规范现场检查指导原则(2016年修订稿)(食药监药化监〔2016〕160号)一、为规范药品经营企业监督检查工作,根据《药品经营质量管理规范》,制定《药品经营质量管理规范现场检查指导原则》。二、本指导原则包含《药品经营质量管理规范》的检查项目和所对应的附录检查内容。检查有关检查项目时,应当同时对应附录检查内容。如果附录检查内容存在任何不符合要求的情形,所对应的检查项目应当判定为不符合要求。
查看详情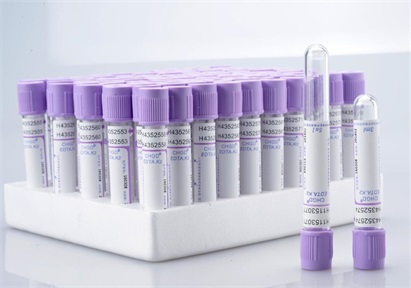
一次性使用真空采血管产品注册技术审查指导原则(食药监办械函[2011]187号)本指导原则旨在指导和规范第二类一次性使用真空采血管的技术审评工作,帮助审评人员理解和掌握该类产品的原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性做出系统评价。本指导原则所确定的核心内容是在目前的科技认识水平和现有产品基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
查看详情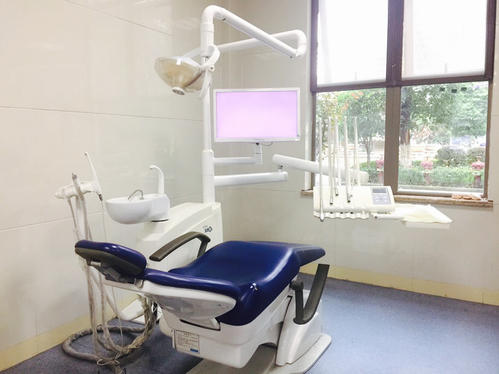
牙科综合治疗机注册技术审查指导原则(2016年修订版)(2016年第22号)本指导原则旨在指导注册申请人对牙科综合治疗机注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对牙科综合治疗机的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
超声理疗设备注册技术审查指导原则(2017年修订版)(2017年第177号)本指导原则旨在指导注册申请人对超声理疗设备(第二类)注册申报资料的准备和撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则系对超声理疗设备注册技术审查的通用要求,医疗器械注册申请人应依据具体产品的特性对注册申报材料的内容进行充实细化。医疗器械注册申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需阐述其理由及相应的科学依据。
查看详情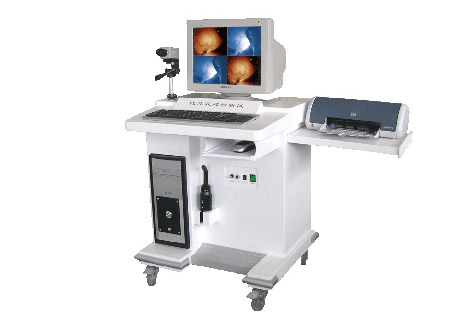
红外乳腺检查仪注册技术审查指导原则(2017年修订版)(2017年第146号)本指导原则旨在指导注册申请人对红外乳腺检查仪注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对红外乳腺检查仪的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
电子血压计(示波法)注册技术审查指导原则(2016年修订版)(2016年第22号)本指导原则旨在指导注册申请人对电子血压计(示波法)注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对电子血压计(示波法)的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
3A类半导体激光治疗机产品注册技术审查指导原则(食药监办械函[2011]187号)本指导原则旨在指导和规范3A类半导体激光治疗机产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
查看详情
电动病床注册技术审查指导原则(2017年修订版)(2017年第30号)本指导原则旨在规范和明确电动病床产品技术审评过程的审查要求,并为注册申请人提交电动病床产品申报资料提供具体指导。本指导原则中不包括行政审批要求,不作为法规强制执行,应在遵循相关法规的前提下使用本指导原则。
查看详情