24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

磁疗产品注册技术审查指导原则(2016年修订版)(2016年第22号)本指导原则旨在指导注册申请人对磁疗产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对磁疗产品的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
椎间融合器注册技术审查指导原则(2016年第70号)椎间融合器作为骨科植入性医疗器械,是实现脊柱相邻椎间隙融合的主要植入物之一,其安全性和有效性直接影响相邻椎体骨性融合的效果。本指导原则旨在指导注册申请人对椎间融合器的产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则系对椎间融合器的一般要求,申请人应依据具体产品特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情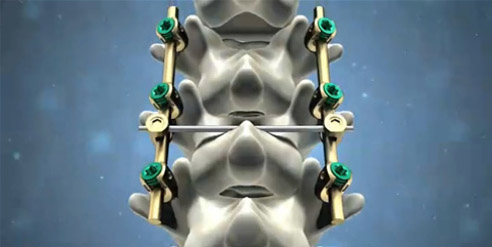
脊柱后路内固定系统注册技术审查指导原则(2016年第70号)脊柱手术目的是矫正脊柱畸形、缓解疼痛、稳定脊柱和保护神经,脊柱后路内固定术是主要治疗的手段之一,其手术中使用的脊柱后路内固定系统产品的安全性和有效性直接影响着疾病的治疗效果。本指导原则旨在指导为注册申请人对脊柱后路内固定系统产品的注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情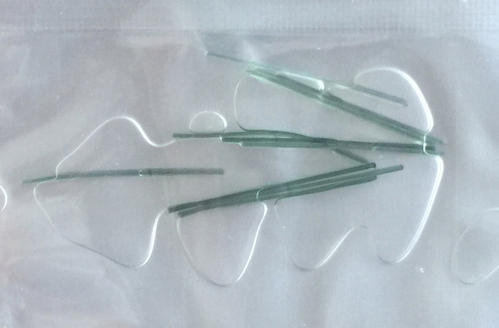
可吸收性外科缝线注册技术审查指导原则(2016年第70号)本指导原则旨在指导注册申请人对可吸收性外科缝线产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情
一次性使用脑积水分流器注册技术审查指导原则(2016年第70号)本指导原则旨在指导注册申请人/生产企业对一次性使用脑积水分流器注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情
牙科基托聚合物材料注册技术审查指导原则(2016年第70号)牙科基托聚合物材料是制作义齿基托和正畸基托的聚合物基材料,本指导原则旨在指导注册申请人对牙科基托聚合物材料的产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情
牙科种植体(系统)注册技术审查指导原则(2016年修订版)(2016年第70号)本指导原则旨在指导注册申请人对牙科种植体(系统)的产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对牙科种植体(系统)的一般要求,申请人应当依据具体产品特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
查看详情
一次性使用输注器具产品注册技术审查指导原则(食药监办械函[2011]116号)本指导原则旨在帮助和指导申请者/生产企业对一次性输注器具产品注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工作的质量和效率。本指导原则是对一次性使用输注器具产品注册申报资料的一般要求,申请者/生产企业应依据具体产品的特性对注册申报资料的内容进行充实和细化,并依据具体产品的特性确定其中的具体内容是否适用。
查看详情