24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
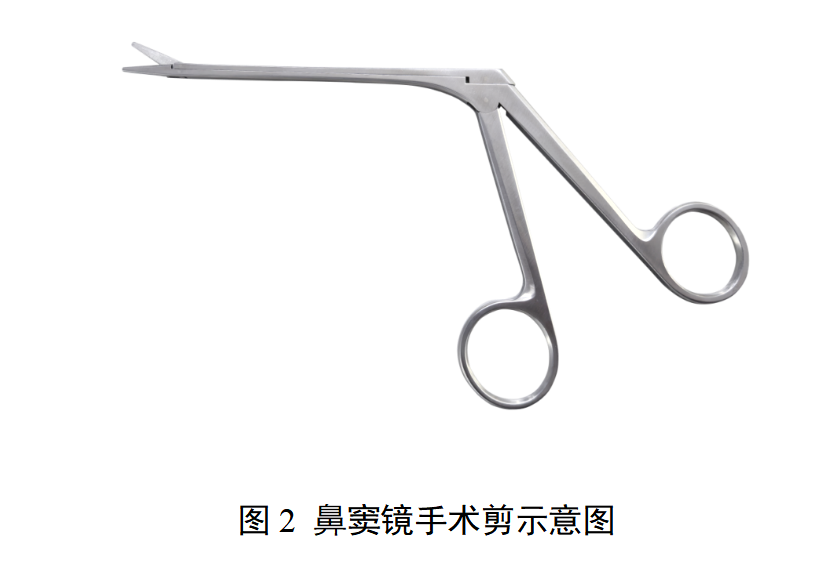
本指导原则旨在为注册申请人进行无源手术器械中内窥镜手术用剪的注册申报提供参考,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对无源内窥镜手术用
查看详情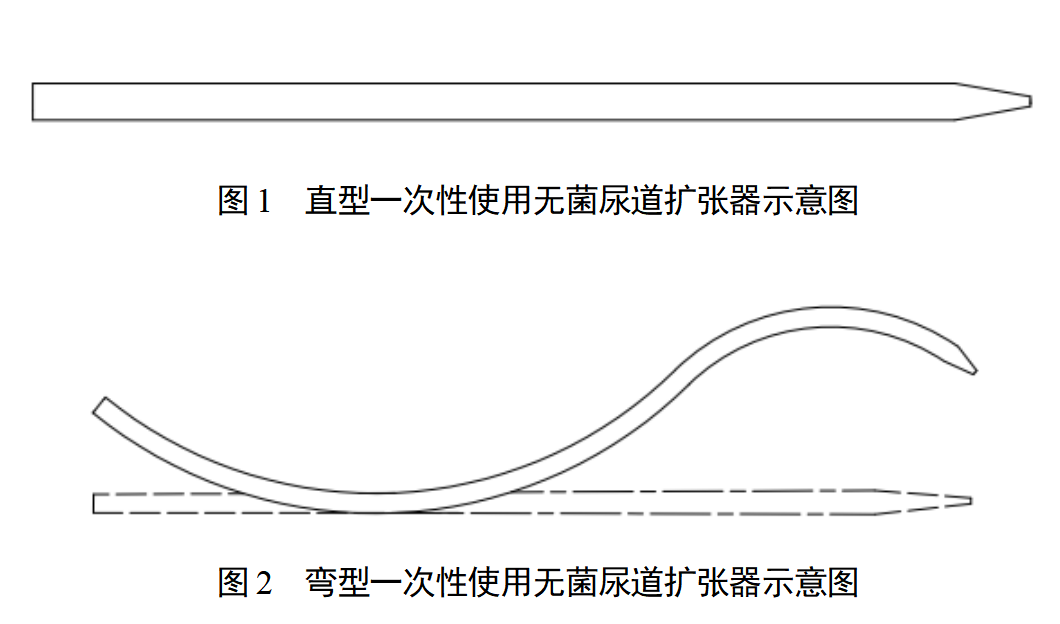
本指导原则旨在帮助和指导注册申请人对一次性使用无菌尿道扩张器注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对一次性使
查看详情
本指导原则旨在为医疗器械注册申请人进行胃镜润滑液注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。 本指导原则是对胃镜润滑液注
查看详情
针对医疗器械企业在进行生产许可申报这一操作之时,所涉及到的生产地址范畴这一关键问题,究竟是否应该将具有特定功能性质的研发区域以及具备办公用途性质的办公区域,依据相
查看详情
医疗器械注册申报这一被定义为严谨而复杂的过程以通过涵盖各个关键方面诸如完整的研究资料去证明产品所具备的安全性以及有效性为核心,依据国家药品监督管理局颁布的相关
查看详情
2025年8月,上海市药品监督管理局共批准首次注册医疗器械产品65项(具体产品见附件)。 特此通告。 附件:2025年8月批准注册医疗器械产品目录 上海市药品监督管理局
查看详情
在药品与医疗器械行业正面临监管态势趋于严格这一背景之下,那被称之为GMP(也就是药品生产质量管理规范)的体系认证,已然成为了企业为能够确保其产品质量、满足法规所规定
查看详情
本指导原则旨在指导注册申请人对牵引床注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对牵引床的一般要求,申请人应依据产品
查看详情