24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

近日,国家药品监督管理局经审查,批准了山东吉威医疗制品有限公司生产的创新产品“优美莫司涂层冠状动脉球囊扩张导管”注册。 优美莫司涂层冠状动脉球囊扩张
查看详情
一、医疗器械分类 在我国,医疗器械按照风险程度分为三类。 第一类风险程度低,实行常规管理可以保证其安全、有效的医疗器械。仅需备案管理。 第二类具有中度风险,需要
查看详情
医疗器械临床试验开展顺序一般为:申办者完成临床前相关研究,选择已备案的医疗器械临床试验机构及主要研究者,并组织临床试验方案等相关文件制定。伦理委员会审查批准该临床
查看详情
2022年8月,国家药品监督管理局共批准注册医疗器械产品210个。其中,境内第三类医疗器械产品161个,进口第三类医疗器械产品25个,进口第二类医疗器械产品22个,港澳台医疗器械产
查看详情
一、单纯疱疹病毒结构 单纯疱疹病毒(Herpes simplex virus ,HSV)是最早发现的人类疱疹病毒,也是人类病毒性疾病中最常见的病毒。HSV感染导致的单纯疱疹是一种常见的传染性
查看详情
本指导原则旨在为医疗器械注册申请人进行牙科根管润滑剂/清洗剂的注册申报提供技术指导,同时也为医疗器械监督管理部门对注册申报资料的审评提供技术参考。 本指导原
查看详情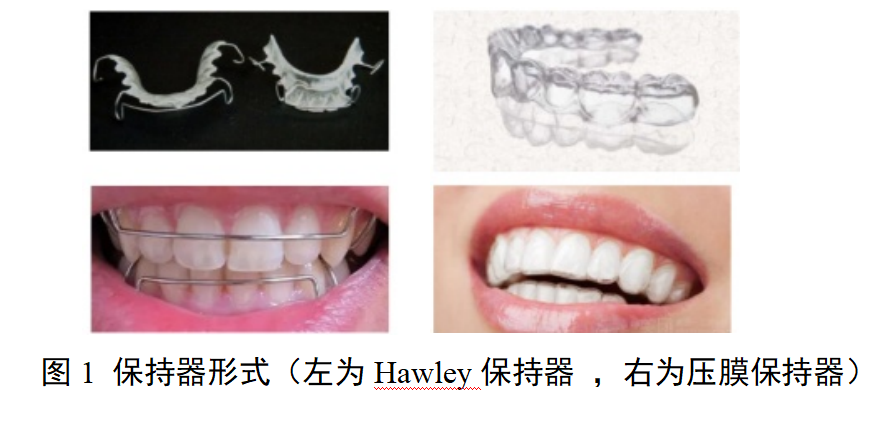
口腔保持器注册审查指导原则
本指导原则旨在指导注册申请人对口腔保持器注册申报资料的准备及撰写,同时也为技术审评部门审评提供参考。 本指导原则是对口腔保持器的
真菌(1-3)-β-D葡聚糖测定试剂注册审查指导原则
本指导原则旨在指导注册申请人对真菌(1-3)-β-D葡聚糖测定(Fungus(1-3)-β-D-glucan)试剂注册申报资料的准备