24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
医疗器械产品包装及说明书上所标注的使用期限或失效日期作为保障产品安全有效的重要措施,其对于医疗器械经营企业和使用单位而言是用以判断产品是否处于合规使用状态的关键信息,而医疗机构在采购验收环节所必须进行的查验使用期限或失效日期这一行为,与医疗机构和经营企业均需建立的应当包含真实、准确、完整和可追溯等要求的进货查验记录制度紧密相关,该记录保存期限有着明确规定,其中销售记录需保存至医疗器械有效期满后2年,植入类医疗器械的销售记录则被要求永久保存。
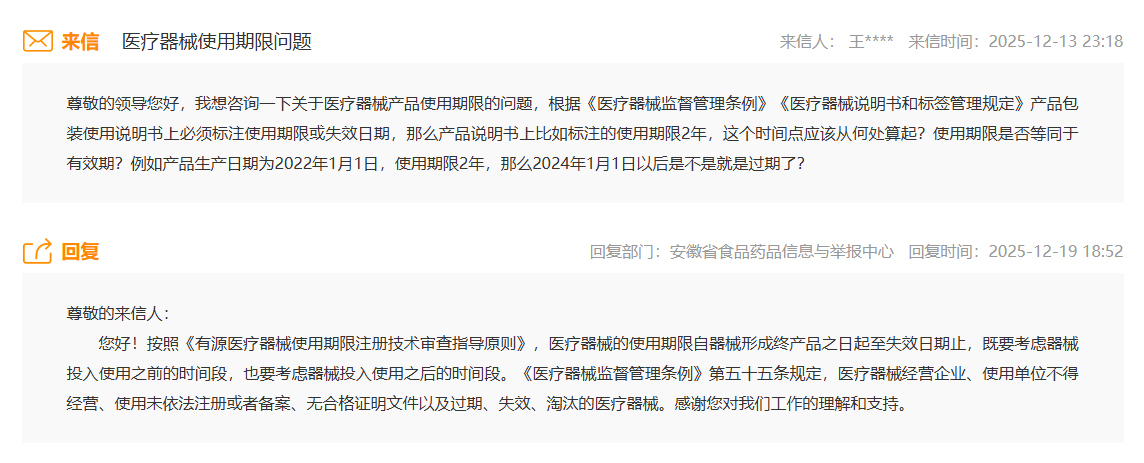
使用期限的起算时间
依据《有源医疗器械使用期限注册技术审查指导原则》可知,医疗器械所规定的使用期限是从器械成为终产品的那个时刻开始,一直到失效日期为止的这段时长,在此过程中不仅要将器械投入使用之前所经历的时间段纳入考虑范围,而且还需对器械投入使用之后的那段时间进行考量,这就表明使用期限的计算起始点为生产日期,而并非是设备正式开始投入使用的那个日期,就像有这样一个具体的案例能够说明这一点,某款颅内压监护仪的生产日期为2020年11月3日,其使用期限被标注为5年,在这种情况下,不管该设备是否已经投入使用,它的失效日期都确定为2025年11月2日,并且在2025年11月2日之后,该器械就会被认定为过期医疗器械。
使用期限与有效期的关系
当医疗器械注册申请人借助风险管理来保障产品安全有效使用的、等同于有效期的使用期限处于存续状态时产品能够维持其适用范围,而失效日期作为使用期限的终止节点,在该节点之后医疗器械的安全有效性将无法被保证,并且在产品注册申报阶段医疗器械注册申请人需于注册资料里明确产品使用期限同时提供相关验证资料,这些验证资料所涉及的验证方法既包含对产品或关键部件运用加速老化试验开展的前瞻性研究以及对本产品或同类产品经验进行的汇总研究,也涵盖对产品或关键部件采用可靠性评估分析方法、模拟测试方法或其他理论及仿真计算方法所做的研究。
法规对过期器械的禁止性规定
《医疗器械监督管理条例》第五十五条明确作出相关规定,即医疗器械经营企业以及使用单位均不得进行经营、使用未依法完成注册或者备案程序、缺失合格证明文件并且处于过期、失效状态或者属于被淘汰范畴的医疗器械的行为,而针对违反此条款的情形,第八十六条相应设定了处罚措施,具体为若违法生产、经营、使用的医疗器械货值金额不足1万元,将并处2万元以上5万元以下的罚款,若货值金额在1万元以上,则并处货值金额5倍以上20倍以下的罚款,另外医疗器械使用单位对于需要进行定期检查、检验、校准、保养、维护的医疗器械,需依照产品说明书所提出的要求来开展检查、检验、校准、保养、维护工作并做好记录,对于使用期限较长的大型医疗器械,还应当为每一台设备建立使用档案,用以记录其使用情况、维护情况、转让情况以及实际使用时间等相关事项。
实务操作中的注意事项
医疗器械使用单位需从持有合法资质的医疗器械注册人、备案人以及生产经营企业处进行医疗器械的购进操作,在实施购进这一行为之时,应当对供货者所具备的资质情况以及医疗器械相应的合格证明文件展开查验工作,并同步建立起涵盖诸多事项的进货查验记录制度,该记录制度所包含的内容有医疗器械的名称、型号、规格、数量,生产批号、使用期限或失效日期、销售日期,注册人、备案人和受托生产企业的名称,供货者或购货者的名称、地址及联系方式,相关许可证明文件编号等各类事项;而针对那些已经超过使用期限的医疗器械,医疗器械使用单位必须严格依照相关规定进行妥善处置,绝对不允许将其继续用于临床诊疗活动之中。
具体计算示例
以您提及的案例来讲,当产品生产日期为2022年1月1日且使用期限标注为2年时,按照时间推算该产品失效日期为2024年1月1日,而从这一天开始该产品即被视为过期医疗器械;在判断医疗器械是否过期的情形下,需以医疗器械说明书以及标签所标注的使用期限或者失效日期作为依据,就像生产日期为2017年9月20日、使用期限为6年的医疗器械,到2023年9月20日便会过期;医疗器械使用单位于库存管理过程中,需要依照贮存条件、医疗器械有效期限等方面的要求,对所贮存的医疗器械进行定期检查并做好相关记录,以便能够及时发现并且清理过期医疗器械,进而确保所使用的医疗器械处于有效期内。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。