24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
医疗器械软件和医疗器械产品一致,也按医疗器械注册流程走,同样分为二类医疗器械注册和三类医疗器械注册。医疗器械软件在注册后,通常会由于软件维护的要求或者客户的一些定制化要求,导致软件有变更需求?哪么这些变更是通过质量管理体系控制来实现,还是走许可事项变更流程呢?飞速度根据现行的注册法规及审评要求,为大家作一解答。

通常软件的变更需求是客观存在的,对于确认的变更需求,应首先进行变更的风险分析,凡是影响到医疗器械安全性或有效性的软件更新均为重大软件更新。具体而言,软件更新如影响到医疗器械的预期用途、使用环境或核心功能,即属于重大软件更新。包括:
1. 适应型软件更新:指软件运行平台跨越互不兼容的计算平台(包括硬件和软件),如操作系统软件由Windows变为iOS,32位计算平台变为64位计算平台、常规计算平台变为移动计算平台等;
2. 完善型软件更新:影响到用户临床决策(包括决策能力、决策结果、决策流程和用户临床行动),或者影响到人员安全(包括患者、用户和其他相关人员),包括但不限于:
(1)临床功能改变,如新增临床应用、新增运行模式、采用新核心算法等;
(2)软件输出结果改变,如医学图像或数据质量改变、用户界面增加临床信息等;
(3)用户使用习惯改变,如用户原有临床工作流程改变、用户界面布局改变等;
(4)影响到患者安全,如采用新的软件安全标准、用户界面增加报警信息等。
其它如核心算法导致运算速度的单纯性提高、临床工作流程的可配置化(即用户可以保留原有临床工作流程)、用户界面的文字性修改,除非影响到医疗器械的安全性或有效性,一般不视为重大更新。
3. 其他软件更新:软件的安全性级别、体系结构、用户界面关系或物理拓扑发生改变。
需要说明的是:重大软件更新的范围会随着认知水平与技术能力的提高、不良事件与召回事件的分析进行动态调整。
重大软件更新,须进行注册证变更流程并提交软件更新描述文档,包括基本信息、实现过程和核心算法,具体见以下要求。
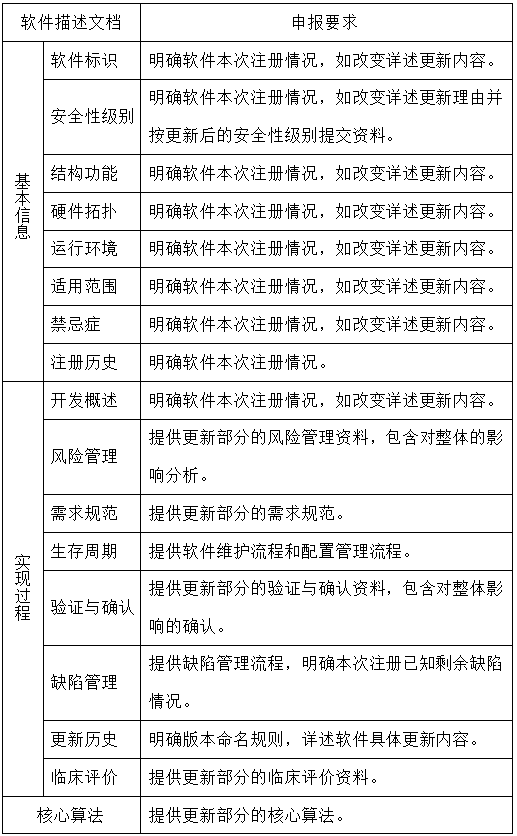
发生轻微软件更新,通过质量管理体系进行控制,无需进行注册变更,待到下次注册或变更时提交相应申报资料。具体细节参考《医疗器械软件注册技术审查指导原则》。
医疗器械软件的重新开发(即制造商弃用原有软件)不属于软件更新,应按照医疗器械产品注册的要求提交注册申报资料。
若您有医疗器械软件注册变更方面的问题,也可以联络我们。我们有专业的软件开发人员与注册团队,可以及时提供有效、高质量的咨询服务!
医疗器械软件注册变更相关服务项:
第二类医疗器械注册变更(许可事项变更)服务
第三类医疗器械注册变更(许可事项变更)服务
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
上一篇:如何界定医疗器械产品的注册类别?