24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
国家对于医疗器械有着严格的分类,而三类医疗器械是最高级别的医疗器械,也是必须严格控制的医疗器械,是指植入人体,用于支持、维持生命,对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。如植入式心脏起搏器、体外震波碎石机、病人有创监护系统、人工晶体、有创内窥镜、超声手术刀、彩色超声成像设备、激光手术设备、高频电刀、微波治疗仪、医用核磁共振成像设备、X线治疗设备、200mA以上X线机、医用高能设备、人工心肺机、内固定器材、人工心脏瓣膜、人工肾、呼吸麻醉设备、一次性使用无菌注射器、一次性使用输液器、输血器、CT设备等。
三类医疗器械产品注册流程
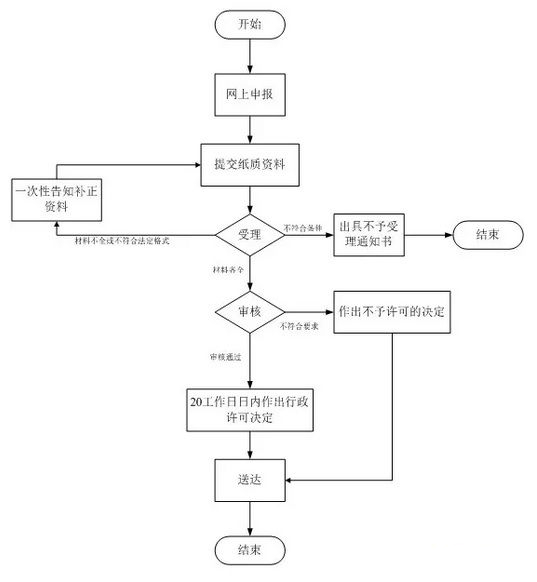
1. 申请:申请人向国家食品药品监督管理总局行政受理服务大厅提出申请。
2. 受理:受理人员根据申报事项按照相关法律法规的要求对申报资料进行形式审查。申请事项属于本部门职权范围,申报资料齐全、符合形式审查要求的,予以受理;申报资料存在可以当场更正的错误的,允许申请人当场更正;申报资料不齐全或者不符合形式审查要求的,在5个工作日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申报资料之日起即为受理;申请事项不属于本部门职权范围的,即时告知申请人不予受理。
3. 审查:受理人员自受理之日起3个工作日内将申报资料转交技术审评机构,技术审评机构应当在90个工作日内完成第三类医疗器械注册的技术审评工作。如果需要外聘专家审评或药械组合产品需与药品审评机构联合审评的,那么所需时间不计算在内,技术审评机构应当将所需时间书面告知申请人。此外,质量管理体系核查的时间和申请人补充资料的时间,也不计算在审评时限内。
4. 许可决定:国家食品药品监督管理总局应当在技术审评结束后20个工作日内作出决定,对符合安全、有效要求的,准予注册。对不予注册的,应当书面说明理由,并同时告知申请人享有申请复审和依法申请行政复议或者提起行政诉讼的权利。
5. 送达:自作出审批决定之日起10个工作日内,总局行政事项受理服务和投诉举报中心将行政许可决定送达申请人。
三类医疗器械产品注册注意事项
1. 送检资料准备
产品技术要求:参考市场上同类产品的性能指标;根据国家标准、行业标准及企业标准制定产品技术要求,产品技术要求不能低于国家标准及行业标准;根据《国家食品药品监督管理总局关于发布医疗器械产品技术要求编写指导原则的通告(第9号)》的要求编制;参考市场上同类产品的性能指标。
说明书和标签样稿:参考市场上同类产品的说明书和标签内容;根据CFDA 6号令的要求编制。
检测合同。
2. 确定检验机构资质
承检资质:根据产品的名称和技术要求编写参考的标准确定检验机构是否有承检资质。
确定检验机构后:了解检验机构检测周期,试验用样品量。
3. 检测样本准备
根据《医疗器械生产质量管理规范》的要求生产样品,并自检合格,检测用样品的批号需一致。若产品需要进行临床试验,最好保证临床试验用样品的批号和检测用批号一致。因此建议检测用样品量生产多一点。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。