24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
加速老化试验是医疗器械注册项目重要事项之一,多数医疗器械注册产品采用加速老化试验确定产品效期,本文带大家了解加速老化试验流程和要求。
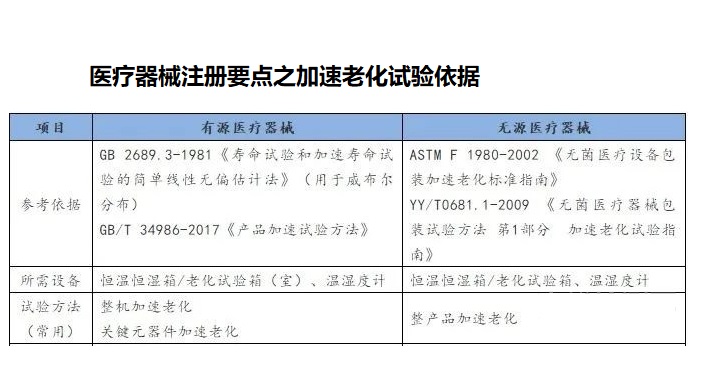
一、为什么要做加速老化试验?
材料物理性能随时间的降低或粘接和热封处的材料随时间的降解以及在随后的运输和搬运中的动态事件,可能会导致无菌屏障系统完整性的丧失,实时老化程序为确保无菌屏障系统材料和无菌屏障系统完整性不随时间而降解提供了最佳数
据。但由于产品更新换代较快,一般采用加速老化研究代表实时老化效应。
加速老化试验研究所得到的数据是基于对材料老化效果的模拟。在无菌屏障系统实时老化研究完成之前只是暂时的。但采用加速老化方案的稳定性试验,在实际老化数据出具之前应被视为标称有效期的充分证据。为了确保加速老化研究能真实地代表;实时老化效应,加速老化应与实时老化研究同步进行(且实时老化的开展不超过加速老化开展的3个月)。实时老化研究应进行至产品标称的货架寿命,并直至完成。
二、加速老化试验流程和步骤?
1.选择加速老化因子值;
2.确定无菌屏障系统货架寿命;
3.确定老化试验的时间间隔,包括零时刻;
4.确定试验条件,环境温度和加速老化温度;
5.决定老化研究中是否采用湿度条件;
6.计算试验持续时间;
7.定义无菌屏障系统的材料特性、密封强度和密封完整性试验、样本量和接受准则;
8.在加速老化温度下对样本进行加速老化,并同步进行实时老化试验;
9.评价加速老化后无菌屏障系统与最初无菌屏障系统要求相应的性能;对实时老化后无菌屏障系统是否满足其最初设计要求进行评价。
三、加速老化试验需要哪些设备?
1.老化试验房间/老化试验箱:使产品独立地暴露于选定的温度和相对湿度的循环空气气中。
2.控制仪器:能使房间(箱)在极限偏差内保持所需大气条件。
3.湿度计:用于指示相对湿度的设备,其相对湿度精度宜为+2%。
4.温度计:可使用任何精度为0.1°C的能记录和显示温度的测量装置。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。