24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

经导管治疗二尖瓣反流技术,目前除了雅培的MitraClip和爱德华的PASCAL,这两款经导管的缘对缘修复技术之外其它治疗技术都非常不成熟,无论是置换还是修复。
然而二尖瓣返流(MR)是最

医疗器械紧急使用管理规定(试行)(征求意见稿) 第一条【制定依据】 为做好特别重大突发公共卫生事件和其他严重威胁公众健康的紧急事件应急处置,指导规范医疗器械紧急
查看详情
长期以来,随机对照试验(RCT)作为强有力的临床数据,一直是评价药物安全性和有效性的金标准,但由于较高的患者纳入和排除标准,试验结果排除了一部分现实世界临床治疗中的患者
查看详情
药物临床试验会涉及对受试者医疗健康信息等个人信息的处理。医疗健康信息具有敏感性,一旦被泄露或被非法使用,容易导致个人的人格尊严或人身、财产安全受到侵害。因此,2021
查看详情
一、中医器械标准 中医器械是指在诊疗活动中,在中医理论指导下应用的仪器、设备、器具、材料及其他物品(包括所需软件)。二、中医器械工作原理
中医诊断设备 脉诊设备
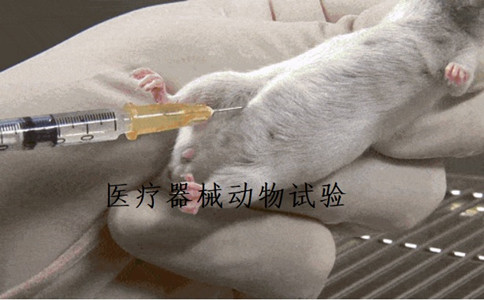
对于医疗器械注册?产品,特别是高风险医疗器械来说,动物实验有助于产品在人体试验前的研究定型及风险预期,本文说一个动物实验的知识点,即医疗器械动物试验是否需要设计对照。
查看详情
对于病毒保存液备案产品来说,通常由灭活型和非灭活型,这两个微生物学的专业名词,有什么区别呢,本文来为大家科普一下。
查看详情
2022年10月29日,陆奇博士最新演讲里面有句话:“所有行业,都值得用数字化重做一遍”,IT行业与医疗行业的结合催生了许多具有临床应用价值的医疗器械软件产品,许多带测量功能医疗器械软件产品。今天,一起来了解带测量功能医疗器械软件注册?注意事项。
查看详情