24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

为确保医疗器械的质量以及临床医疗使用的安全、有效,必须对其生产过程中涉及到的非活性材料进行生物相容性评价,以用于生产工艺过程的监控及最终产品的放行。因此,生物相容性评价是生物材料研究中始终贯穿的主题,也是相关产品生产企业必须关注的问题,本文就整理了生物相容性评价中的相关要点,供大家参考。
查看详情
对于我们大多数普通人来说,如何获得成功,只能“拼自己”。“拼自己”的方式有两种,一种是“孺子牛”(拼命工作不请示不汇报),另一种是“望天猴”(认真工作常请示勤汇报)。
查看详情
我们在说,如果我们以后做药物警戒,做药物临床试验的工作,我的职业生涯怎么发展可能更好,我们一定要深入的思考,一定要非常谨慎的,认真的去思考我们做的这个事情到底该怎么做,几位老师提到了保护患者安全,你怎么保护的?...
查看详情
试验用药,即IP(Investigational Product),指在临床试验中用作试验药或对照药的活性药物或安慰剂的药物制剂,包括已批准上市药物应用于新的应用途径或组合(制剂或包装)、应用于新的适应症或用于收集已批准用法的更多信息。
查看详情
2020年国家局共对89家医疗器械生产企业进行了飞行检查,其中44家IVD企业,16家无菌产品企业,11家有源器械企业,9家植入产品企业,3家义齿企业,3家独立软件企业和其它3家企业。飞行检查原因为合规检查、专项检查、抽检不合格、投诉举报和出现不良事件情况。检查结果为63家企业限期整改,12家停产整改,8家检查前已经停产和1家注销,其中检查不合格项687条,主要集中在生产管理、厂房与设施、设备及质量控制等环节。
查看详情
大概大家都知道,医疗器械在上市销售前,都要到药监局进行登记备案,因为这样对所用医疗器械的安全性、有效性进行系统的评估,以决定是否同意其销售、使用。分国内医疗器械登记和国
查看详情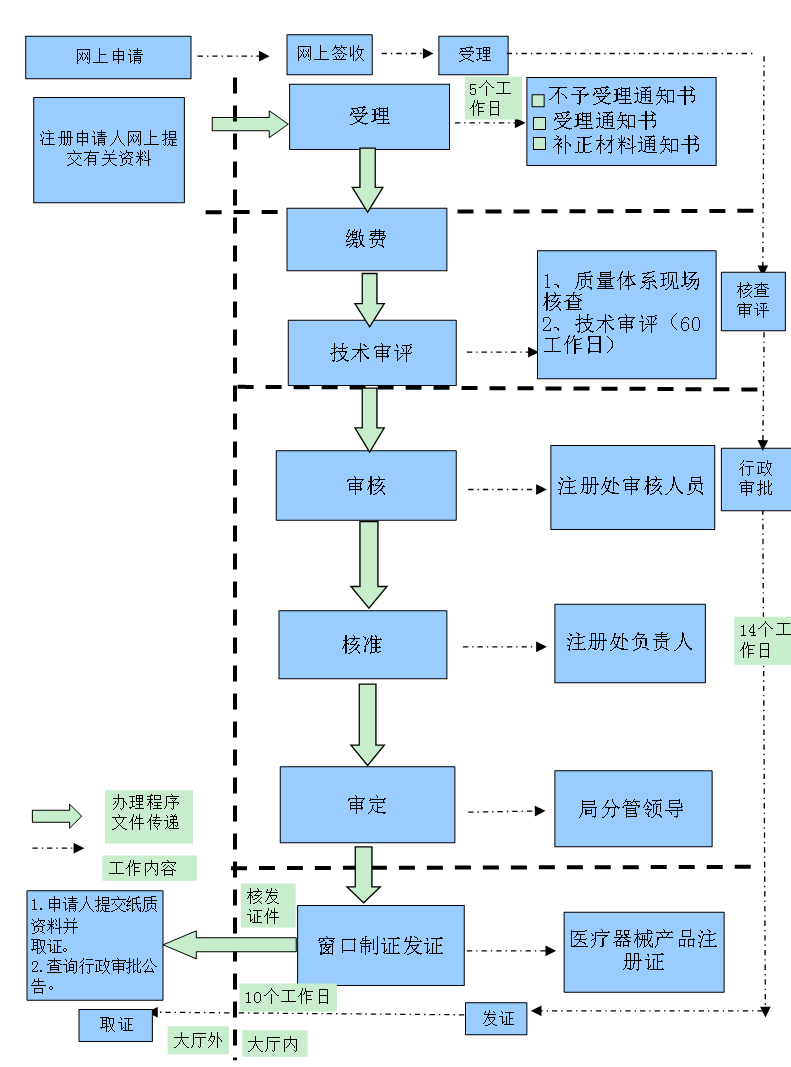
二类医疗器械注册证代办周期1、法规背景《医疗器械监督管理办法》明确规定:从事第二类、第三类医疗器械生产的,生产企业应当向所在地省、自治区、直辖市人民政府食品药品监督
查看详情
飞速度提供佛山二类医疗器械临床试验代办服务!如果你需要把医疗器械临床试验外包的话,可以找我们来完成,专业公司做专业事,更快速!目前,佛山市陆续与高校、研究机构展开合作,与中山
查看详情