24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

注册一个公司都需要很多要求和材料,那么注册二类医疗器械公司都需要什么条件呢?开办第二类医疗器械经营企业许可①企业应具有与经营规模和经营范围相适应的质量管理机构或者专
查看详情
盲法到底是什么?小伙伴们在项目中,经常会看到方案设计使用盲法,那什么是盲法试验,为什么使用盲法?今天我们一起探讨一下临床试验中的盲法以及什么情况下会揭盲。
查看详情
生物相容性是指生命体组织对非活性材料产生反应的一种性能,一般是指材料与宿主之间的相容性。样品是确保检测结果有效性的一个非常重要的环节。那么对于我们常见的生物相容性的测试而言,如何准备样品呢?
查看详情
2020年3月17日国家药监局发布了关于医疗器械主文档登记事项的公告(2021年第36号),之前给大家介绍过医疗器械主文档的主要内容、适用的产品注册类型等信息。今天我们再来向大家介绍一下FDA医疗器械主文档。
查看详情
随机化是临床科研的重要方法和基本原则之一。在科研设计中,随机化方法包括两种形式。第一,随机抽样:指被研究的对象从被研究的目标人群中选出,借助于随机抽样的方法,使目标人群中的每一个体都有同样的机会被选择作为研究对象。第二,随机分组:将随机抽样的样本(或连续的非随机抽样的样本)应用随机化分组的方法,使其都有同等机会进入“试验组”或“对照组”接受相应的试验处理。这样就能使组间的若干已知的或未知的影响因素基本一致,使能被测量和不能被测量的因素基本相等,平衡了混杂因素,减少了偏倚的干扰,增强组间的可比性。
查看详情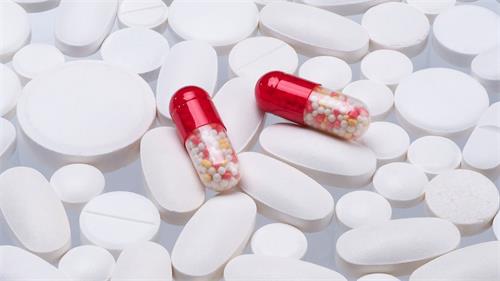
身为患者,我们可能想到的第一个问题就是:什么是药物临床试验?药物临床试验如何进行?我参加药物临床试验,会对我的身体造成影响吗?我参加药物临床试验对我有什么好处?有的患者对于临床试验甚至存在一种误解,觉得参加试验就是当小白鼠。现在,让我们来一一了解这些问题。
查看详情
本文是关于医疗器械临床试验设计的思考问题之一,在主要有效性评价指标的考虑上,更偏向于定性指标还是定量指标?文章文字性内容较多,请耐心查看,一定会对你有所帮助,我们只发干货。

在注册申报前,产品适应症的确定,是医疗器械全生命周期中关键环节。适应症选择应符合相关法律法规、相关指南、伦理等要求,应具有严谨的科学依据。合理的适应症决定了产品的定位,决定了开展临床评价的实施情况、市场推广难易程度等各个环节。确定适应症需要申办者、研究者、机构/伦理、监管部门等多方沟通。
查看详情