24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

2020年9月24日,国家药监局关于发布球囊扩张导管等6项指导原则的通告(2020年 第62号) 。
查看详情
3D打印髋臼杯产品注册技术审查指导原则(2020年第36号)本指导原则旨在帮助和指导注册申请人对3D打印(下称:增材制造)髋臼杯产品注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工作的质量和效率。本指导原则是对增材制造髋臼杯产品注册申报资料的一般性的原则要求,注册申请人/生产企业应依据具体产品的特性对注册申报资料的内容进行充实和细化,并依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
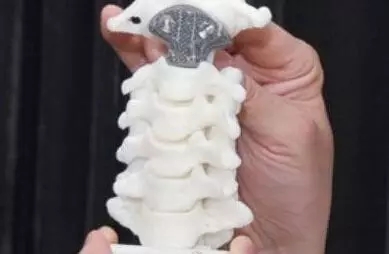
3D打印人工椎体注册技术审查指导原则(2020年第36号)本指导原则旨在帮助和指导注册申请人对3D打印人工椎体产品注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工作的质量和效率。本指导原则系对3D打印人工椎体注册申报资料的一般要求,注册申请人/生产企业应依据具体产品的特性对注册申报资料的内容进行充实和细化,并依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
查看详情
生殖遗传学是一个主要涉及为预测未来怀孕的可能结果进行不同测试,或评估有可能导致怀孕后母亲或孩子患某些疾病的基因变化的医学领域,包括辅助生殖、遗传咨询,以及胚胎植入前、产前和产后筛查和诊断。生殖遗传学医疗器械主要包括试剂、医疗设备、器具以及软件。
查看详情
关于医疗器械注册相关事项多而且繁杂,因此,我们将不断的为大家介绍相关事项,今天为大家介绍医疗器械文档相关知识。
查看详情
医疗器械主文档制度在医疗器械CE认证及其它国家应用较为普遍,我国也在逐步尝试推广使用。感谢药监总局审评老师有关医疗器械主文档制度的前瞻性分享,在此,借花献佛,送给大家。
查看详情
2020年9月29日,药监总局发布关于进口医疗器械注册申报资料试行电子签名有关事宜的通告(2020年第20号),就进口医疗器械注册申报资料试行电子签名有关事宜进行明确,详见正文。
查看详情
今日,药监总局发布关于公开征求《一次性使用注射笔配套用针注册审查技术指导原则(征求意见稿)》意见的通知,就一次性注射笔医疗器械注册审评相关事项面向公众公开征求意见。
查看详情