24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
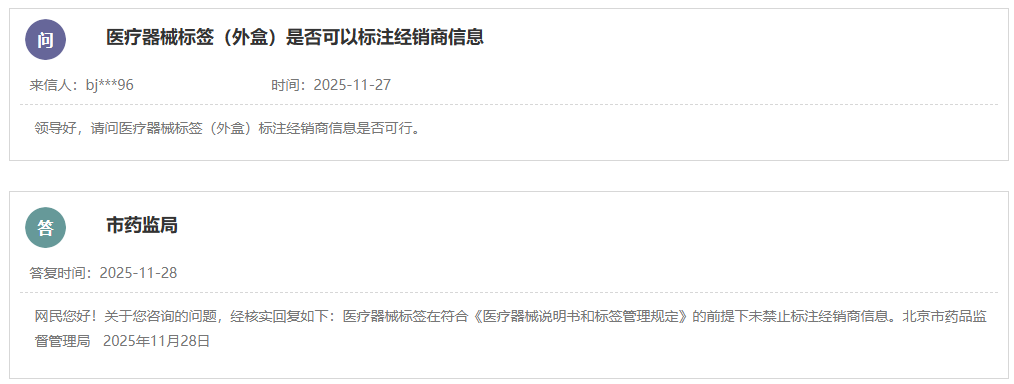
在医疗器械从生产到流通的整个环节之中,标签作为承载着产品身份标识以及安全性信息的关键载体,其内容是否符合相关法规要求,不仅仅会对产品能否顺利进入市场产生直接影响,而
查看详情
当作为医疗器械生产企业的贵公司面临所生产的如有源医疗器械半导体激光治疗机这类产品的注册证将于2025年9月29日到期、却已在2025年3月7日提交延续注册及变更注册申请
查看详情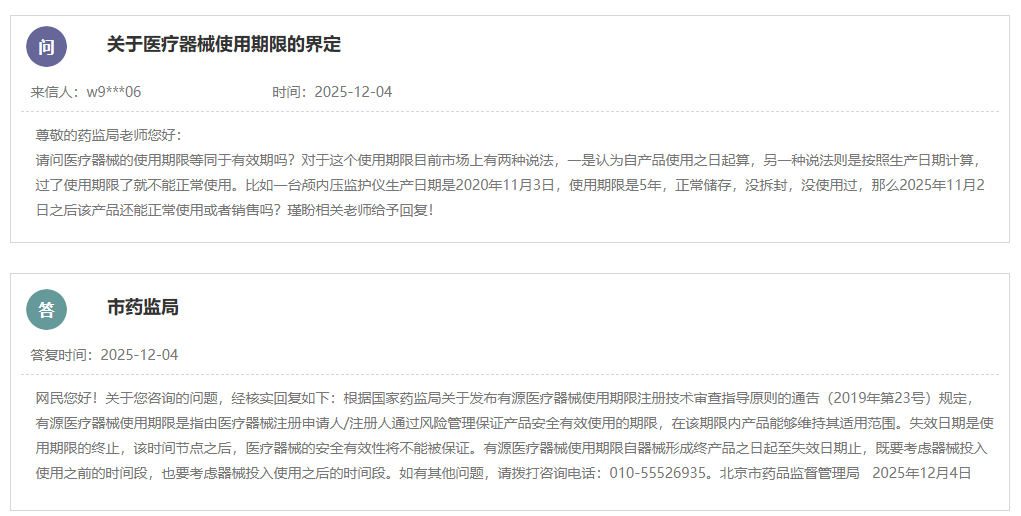
在医疗器械管理与使用的实际操作场景之中常常会出现令人感到困惑的情况,即有关产品“使用期限”究竟应该通过何种方式进行计算以及该“使用期限”是
查看详情
2025年11月,北京市药品监督管理局共批准注册第二类医疗器械产品60个(具体产品见附件)。 特此公告。 附件:2025年11月批准注册第二类医疗器械产品目录 北京市药品
查看详情
二类医疗器械作为风险程度处于中等水平、需经历严格管控流程的产品,其注册流程因涉及分类界定这一明确产品属性的基础环节、技术文件准备这一涵盖详细技术参数与规范的关
查看详情
为了支持罕见病防治医疗器械研发,加快相关产品审评审批,器审中心于2018年发布《用于罕见病防治医疗器械注册审查指导原则》,开辟专门的受理前咨询路径,明确临床试验减免原则
查看详情
本指导原则旨在指导注册申请人对胱抑素C测定试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对胱抑素C测定试剂的一般要
查看详情
本指导原则旨在指导注册申请人对电解质钾、钠、氯、钙四种测定试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对电解质
查看详情