24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

润滑剂类产品在美国根据产品预期用途的不同主要分为人体润滑剂和患者润滑剂:其中,人体润滑剂主要成分为水、丙二醇、羟乙基纤维素、苯甲酸、卡波姆、氢氧化钠等,作用于生殖器,起滋润作用。该类产品在FDA的分类为Ⅱ类,认证途径为510K(Premarket Notification上市前通告)以及产品列名。产品代码为:NUC。
单独此类润滑剂产品在中国不属于医疗器械,但安全套在中国是属于Ⅱ类医疗器械。
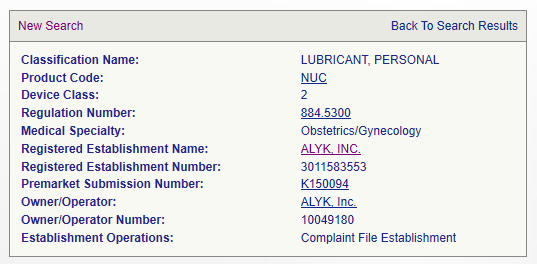
患者润滑剂的预期用途是用于润滑身体自然腔道,以便于诊断或治疗设备进入腔道。该类产品在FDA的分类为I类,认证途径为豁免510K,只需要做产品列名。产品代码为:KMJ。

然而,患者润滑剂此类产品在中国的分类为Ⅲ类或Ⅱ类,其中由二甲基硅油、黄原胶、硅油等成分组成,含有盐酸利多卡因、盐酸丁卡因等药物,无菌提供的,用于内窥镜进入人体自然腔道时的润滑,为药械组合的Ⅲ类医疗器械,品名如:胃镜胶、内窥镜润滑剂。而通常只由甘油、黄原胶等成分组成,不含药物成分的润滑剂产品则为Ⅱ类医疗器械。
人体润滑剂产品在美国FDA需要进行的试验项目有:产品有效期验证、生物相容性测试:细胞毒性(ISO 10993-5: 2009)、阴道刺激试验(ISO 10993-10: 2010)、 豚鼠最大耐受致敏试验(ISO 10993-10: 2010)、急性毒性测试(ISO 10993-11: 2006)以及安全套相容性测试。

美国FDA医疗器械注册业务的办理流程
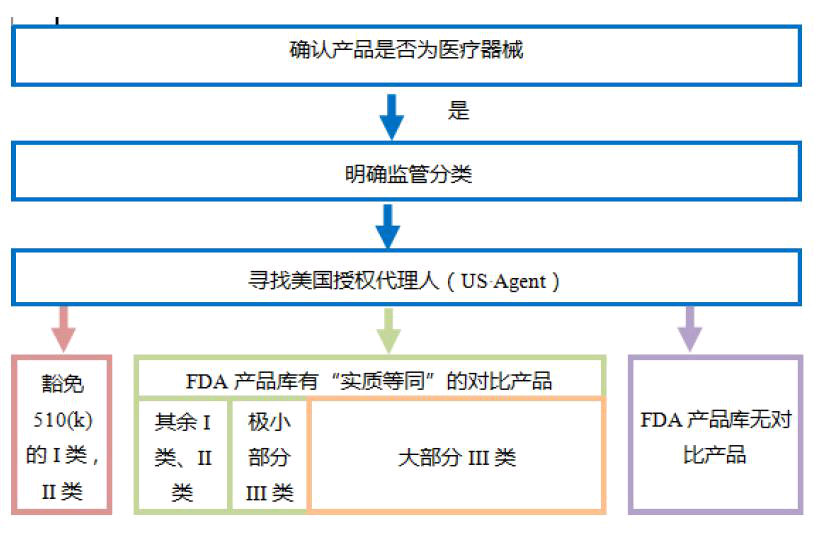
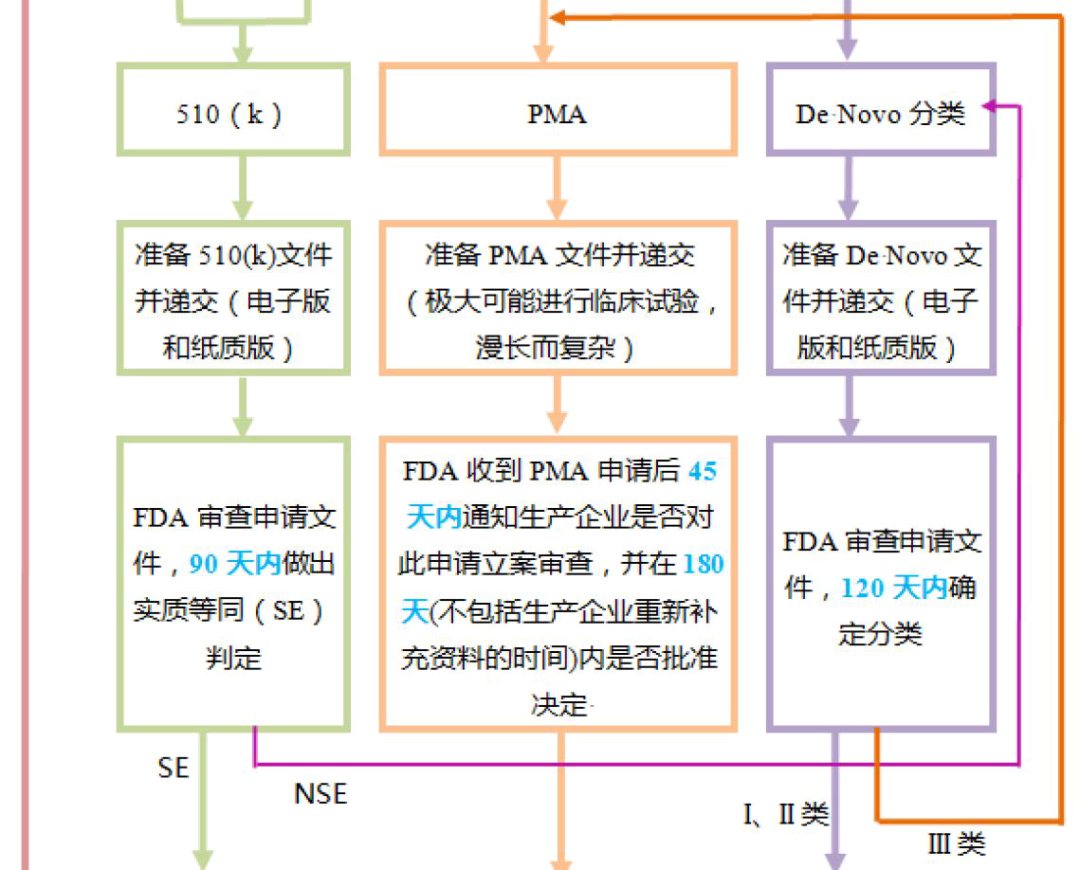

参考信息:
1、www.fda.gov/
2、2018版医疗器械分类目录
如果您对办理美国FDA医疗器械注册的事项还有任何疑问,欢迎咨询客服人员!
来源:金飞鹰
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
上一篇:第一类医疗器械生产备案凭证图片
下一篇:cra首次监查工作经验和收获