24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
引言:任何国家医疗器械产品出口澳大利亚,需经历TGA注册,以下是关于澳大利亚医疗器械注册知识点,简单了解一下,文中大致概括了注册全流程,未标明细节,如有产品需要澳大利亚注册,欢迎联系在线客服。

澳大利亚医疗器械注册知识点汇总
澳大利亚TGA全称是The Therapeutic Goods Administration,是澳大利亚政府卫生部的一部分,负责管理治疗用品,包括处方药、疫苗、防晒霜、维生素和矿物质、医疗设备、血液和血液制品。几乎任何声称具有治疗功效的产品都必须被登记在澳大利亚ARTG,然后才能在澳大利亚供应。
The Therapeutic Goods Administration (TGA) is part of the Australian Government Department of Health, and is responsible for regulating therapeutic goods including prescription medicines, vaccines, sunscreens, vitamins and minerals, medical devices, blood and blood products. Almost any product for which therapeutic claims are made must be entered in the Australian Register of Therapeutic Goods (ARTG) before it can be supplied in Australia.
一、医械产品分类确定
生产商需要提供如下资料以确定医疗器械分类:
The manufacturer is responsible for determining the classification of a device using a set of classification rules based on the:
1.医疗器械的预期用途。
·manufacturer’s intended use of the device
2.对病人,用户及其他人的风险等级。
·level of risk to patients, users and other persons (the probability of occurrence of harm and the severity of that harm)
3.植入人体的程度。
·degree of invasiveness in the human body
4.使用时限。
·duration of use
其分类等级划分如下表:
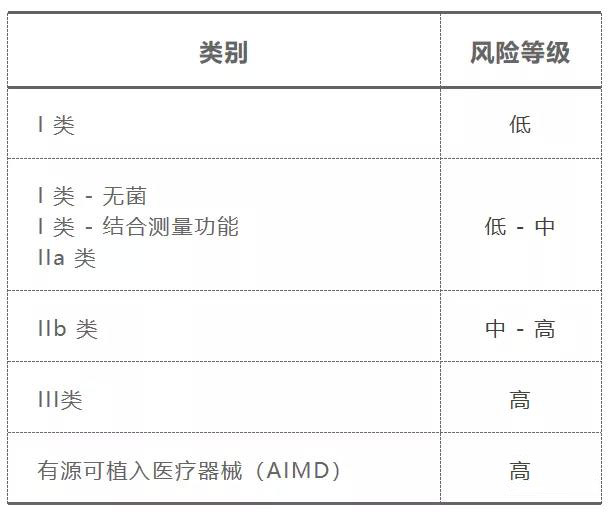
二、符合性评估
什么是符合性评估?
制造商必须能够证明该器械以及制造该器械的过程符合澳大利亚相关法规的要求。
相关法规如下:
1.Therapeutic Goods Act 1989 (the Act)
2.Therapeutic Goods (Medical Devices) Regulations 2002 (the Regulations)
符合性评估证据类型:
The TGA accepts the following certificates as conformity assessment evidence:
1.TGA颁发的符合性评估证书(对部分企业是唯一途径)
a TGA Conformity Assessment Certificate issued by the TGA - this is mandatory for some manufacturers
2.澳大利亚EC MRA 符合性证书
certificates of conformity issued under the Australia -EC MRA
3.澳大利亚 EFTA MRA 符合性证书
certificates of conformity issued under the Australia -EFTA MRA
4.由欧盟公告机构颁发的EC证书
EC certificates issued by an EU Notified Body
符合性评估所需材料:

三、相关费用
1. 注册申请费用
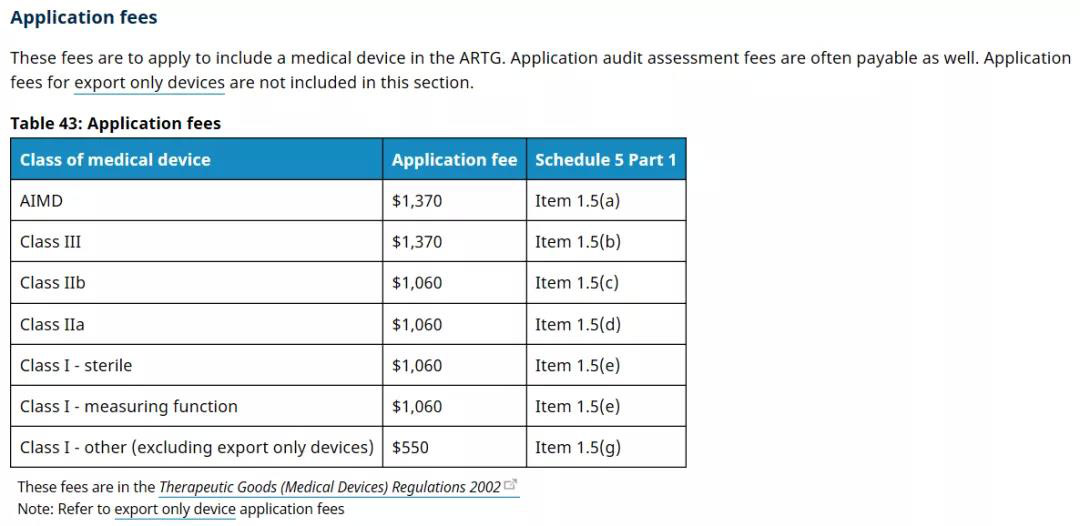
2. 符合性评估费用
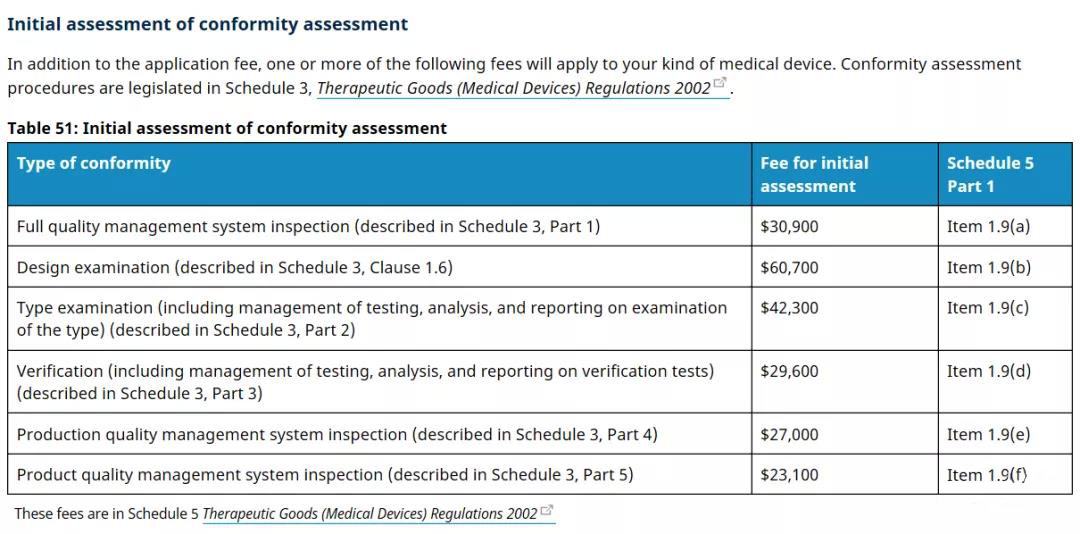
3. 申请核查费用

4. 发证费用
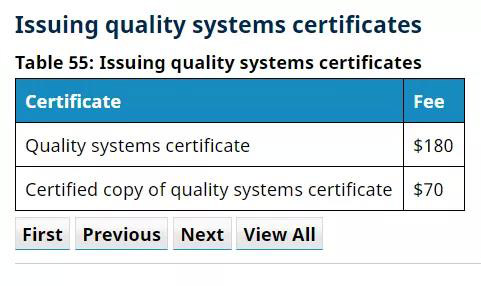

*由官方费用具有可变动性,实际费用以实时价格为准。
四、澳大利亚医疗器械TGA注册流程
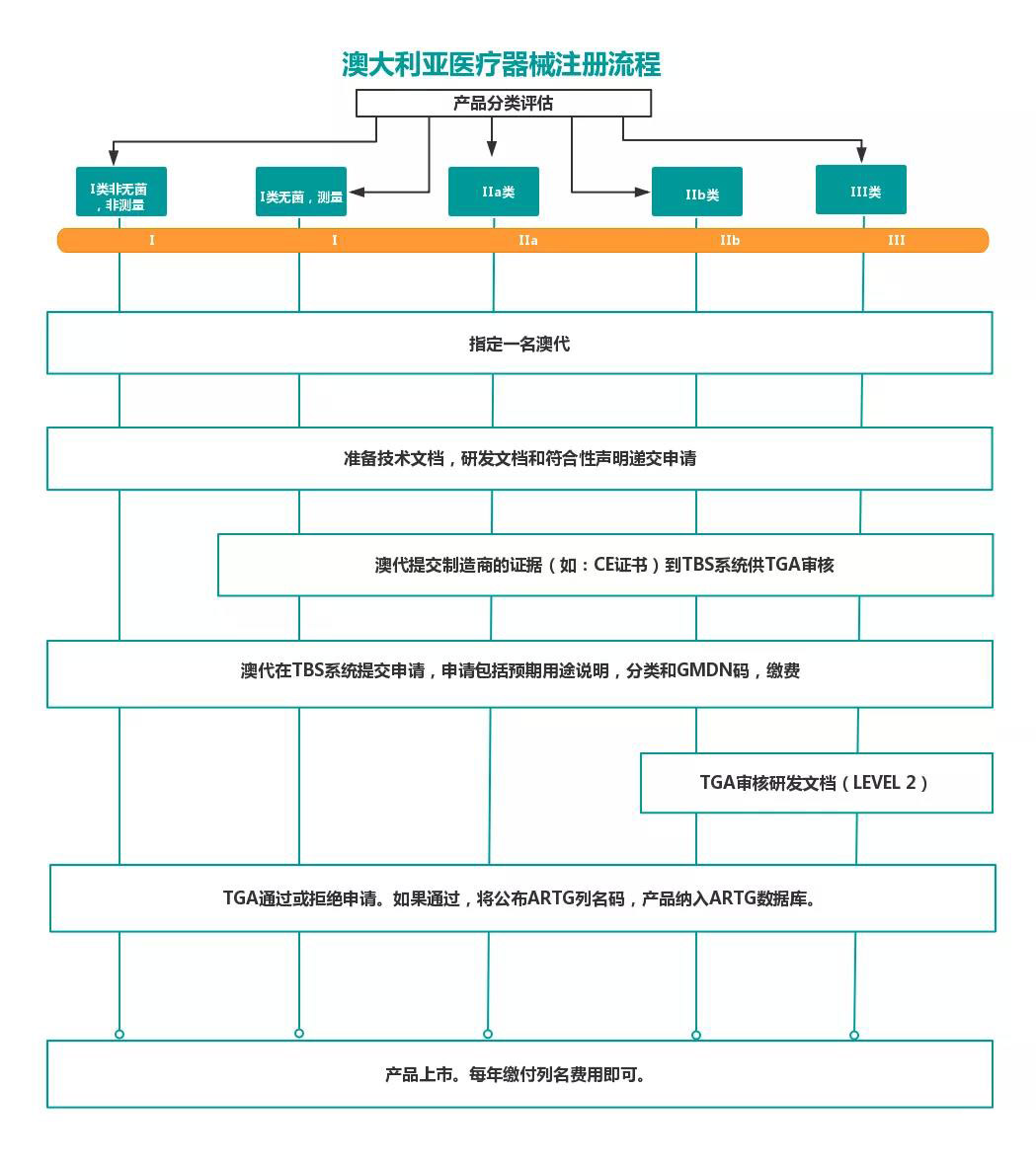
*
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
上一篇:SSU项目合同审核签署阶段的流程