24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

英国已经正式脱欧,那么从2021年1月1日起,医疗器械进入英国境内,就需要申请“UKCA”。
UKCA产生的大背景是英国脱欧。英国脱欧后,不再沿用之前欧盟框架下的市场准入的法规和制度,而建立英国自身的市场准入法规和制度。因此产生了UKCA认证标志。从下图可以看出,英国脱欧的过渡期将在2020年12月31日结束。从2021年1月1日后,UKCA标志就启用了。UKCA标志覆盖很多领域,基本上包含了原CE新方法指令的所有范畴。本系列文章主要讨论的是医疗器械领域,包括通用医疗器械、体外诊断医疗器械以及有源植入性医疗器械。
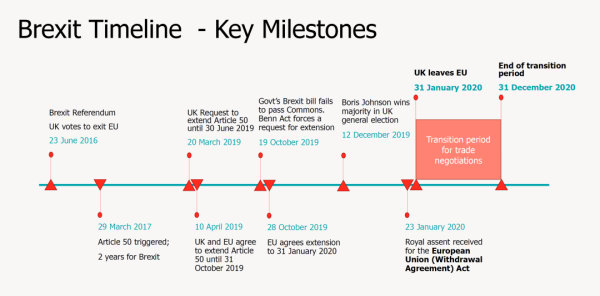
UKCA是什么,即英国合格评定,是英国产品符合性标识,不过此标识只适用于英格兰、苏格兰和威尔士,不适用于北爱尔兰。
突然要用UKCA标识,很多企业来不及办理呀,别急,这里给的有过渡期,从2021年起,到2023年6月30日,进入英国的产品可以继续使用CE标识,不必须用UKCA标识,但是从2023年7月1日起,就必须使用UKCA标识。
UKCA过渡期到底是2021年1月1日,还是2023年7月1日?两个过渡期都对,但理解不同。在2021年1月1日前没有取得CE的产品,该日后需强制认证UKCA,单独认证CE就无法进入英国市场。已经取得CE认证的医疗器械产品,可以沿用到2023年,到2023年7月后,强制认证UKCA。
医疗器械的加贴UKCA标志的要求,总体上可以分为UKCA合格评定和MHRA注册申报两大模块。英国MHRA在今年9月初和12月初分别发布了针对2021年医疗器械制造商如何将产品合法的投放英国市场的指南文件。这两份文件对于制造商的合规日期有明确的表述。
UKCA合格评定
1)对于目前持有公告机构签发CE证书的制造商,在 2023年6月30日,可以继续使用CE证书将产品出口到英国(UK)市场。在2023年6月30日之后,还可以继续出口到英国的北爱尔兰(NI)市场,而不再能出口到GB(英格兰、苏格兰和威尔士)市场。所以,从2023年7月1日开始,原来需要通过公告机构CE证书出口的医疗器械,要继续出口到GB市场,需要取得获认可的英国认证机构签发的UKCA的证书。
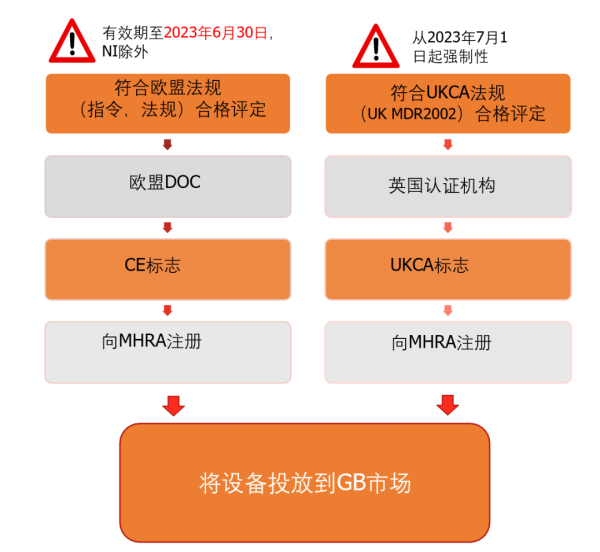
2)对于自我宣告类产品(依据MDD指令和IVDD指令),在2021年1月1日开始就可以按照UK MDR 2002的要求来准备技术文件和相关支持性材料,以完成自我宣告,加贴CE标记。
1、申请UKCA标识
不同的产品有不同的方式,比如:
普通一类MD和普通IVD的,不需要公告机构介入,只需要做自我申明,但是制造商必须做产品测试和提供技术文档;
I类灭菌和I类测试的,做自我申明的同时,还需要公告机构介入,而且制造商必须做产品测试和提供技术文档;
2、进行MHRA注册
进行MHRA注册,通过注册在英国境内的代理人来做注册。MHRA更新了器械注册的规定,在脱欧之前,需要在MHRA注册的器械只包括一类器械,通用类的IVDD以及定制器械。但是脱欧后,MHRA要求所有类别的医疗器械都需要在MHRA进行注册。不过MHRA英国政府依据不同的产品给出了为期一年的过渡宽限期,基于产品风险等级高低,分别是4个月,8个月和12个月。详细信息如下:
(1)IIb类可植入医疗器械、III类医疗设备、有源植入类医疗器械及IVD列表A的宽限期到2021年4月30日(4个月);
(2)IIb类非植入式医疗设备、IIa类医疗器械、IVD列表B、自测IVD的宽限期到2021年8月31日(8个月);
(3)I类医疗器械、普通IVD的宽限期到2021年12月31日(12个月)。
可以看出,对于一类医疗器械和通用类的体外诊断的时间是2021年12月31日。那么对于之前在MHRA注册过的器械,我们该如何处理呢?MHRA的指南文件给出了如下信息:
(1)对于原本就有注册义务的,不适用该过渡期;MHRA在12月7日更新的文件进一步表述了这个指的是英国境内的制造商,以及签约欧盟授权代表是位于爱尔兰的境外制造商。
(2)原来通过欧盟授权代表在英国MHRA进行的注册,在2021年1月1日起全部失效。需要重新指定英国代表,重新申报注册。
(3)英国境外的制造商应尽早指定英国代表。
UKCA证书

总结
从上述信息,我们不难看出对于中国的医疗器械制造商,如果你需要继续出口英国市场,那么尽早指定英国代表,并在新的UKCA框架下完成MHRA注册是必须的。同时,还应关注你的产品的风险等级,以及之前获取CE证书的情况,来策划满足UKCA要求的时间和路径。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。